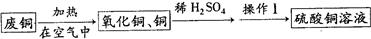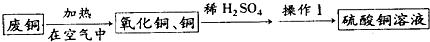题目内容
某活动小组用废铜制取硫酸铜溶液,实验过程为:

(1)氧化铜与稀硫酸反应的化学方程式为
(2)操作Ⅰ的名称是
(3)盛放硫酸铜溶液不宜用铁制容器的原因(用化学方程式解释)

(1)氧化铜与稀硫酸反应的化学方程式为
CuO+H2SO4=CuSO4+H2O
CuO+H2SO4=CuSO4+H2O
.(2)操作Ⅰ的名称是
过滤
过滤
,该操作用到的玻璃仪器有:玻璃棒、烧杯、漏斗
漏斗
.(3)盛放硫酸铜溶液不宜用铁制容器的原因(用化学方程式解释)
Fe+CuSO4═FeSO4+Cu
Fe+CuSO4═FeSO4+Cu
.分析:(1)书写复分解反应的化学方程式时要首先判断能否反应,然后正确书写反应物和生成物的化学式,配平并注明条件.
(2)过滤是分离固体(铜)与液体(硫酸铜溶液)混合物的一种方法.过滤操作用到的主要仪器要记住,特别是玻璃仪器,有烧杯,玻璃棒和漏斗.
(3)盛放硫酸铜溶液不宜用铁制容器是因为铁和硫酸铜溶液反应.
(2)过滤是分离固体(铜)与液体(硫酸铜溶液)混合物的一种方法.过滤操作用到的主要仪器要记住,特别是玻璃仪器,有烧杯,玻璃棒和漏斗.
(3)盛放硫酸铜溶液不宜用铁制容器是因为铁和硫酸铜溶液反应.
解答:解:(1)氧化铜与稀硫酸反应的反应物是氧化铜和硫酸写在等号的左边,生成物是硫酸铜和水写在等号的右边,所以化学方程式为 CuO+H2SO4=CuSO4+H2O.
(2)操作Ⅰ的名称是过滤,该操作用到玻璃仪器,有烧杯、玻璃棒和漏斗.
(3)因为铁比铜活泼,能与硫酸铜溶液反应,反应物是铁盒硫酸铜写在等号的左边,生成物是硫酸亚铁和铜,写在等号的右边,所以化学方程式为:Fe+CuSO4═FeSO4+Cu
答案:(1)CuO+H2SO4=CuSO4+H2O;(2)过滤,漏斗;(3)Fe+CuSO4═FeSO4+Cu.
(2)操作Ⅰ的名称是过滤,该操作用到玻璃仪器,有烧杯、玻璃棒和漏斗.
(3)因为铁比铜活泼,能与硫酸铜溶液反应,反应物是铁盒硫酸铜写在等号的左边,生成物是硫酸亚铁和铜,写在等号的右边,所以化学方程式为:Fe+CuSO4═FeSO4+Cu
答案:(1)CuO+H2SO4=CuSO4+H2O;(2)过滤,漏斗;(3)Fe+CuSO4═FeSO4+Cu.
点评:本题考查了同学们的分析能力还有书写化学方程式的能力.

练习册系列答案
相关题目