题目内容
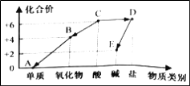
【题目】某工厂化验室用10%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸(该产品中其它物质不与NaOH反应),消耗氢氧化钠溶液的质量与反应过程中溶液的pH值关系如图所示。
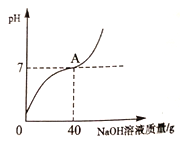
(1)图中A点表示的意义是____________________。
(2)A点消耗氢氧化钠溶液的溶质的质量为___________g。
(3)求石油产品中残余硫酸的质量___________g(写出计算过程)。
【答案】 酸碱恰好中和 4 4.9g
【解析】(1)图中A点的pH=7,说明氢氧化钠和稀硫酸恰好完全反应;
(2)40g氢氧化钠溶液中溶质的质量为:40g×10%=4g;
(3)设石油产品中硫酸的质量为x
2 NaOH+ H2SO4= 2H2O+ Na2SO4
80 98
4g x
![]() =
=![]() ,解得x=4.9g
,解得x=4.9g

练习册系列答案
相关题目
【题目】一些食物的近似pH如下:
食物 | 葡萄汁 | 苹果汁 | 牛奶 | 鸡蛋清 |
pH | 3.5~4.5 | 2.9~3.3 | 6.3-6.6 | 7.6~8.0 |
下列说法正确的是
A. 鸡蛋清和牛奶显碱性 B. 要补充维生索可以多吃鸡蛋清
C. 苹果汁的酸性比葡萄汁弱 D. 胃酸过多的人应少饮葡萄汁和苹果汁