题目内容
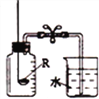
【题目】如图所示,在盛有水的烧杯中,等质量的铁圈和银圈的连接处吊着一根绝缘的细线(两圈不接触),使之平衡,小心地从烧杯中央滴入硫酸铜溶液,观察到的现象是
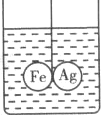
A. 铁圈和银圈左右摇摆 B. 保持平衡
C. 铁圈向下倾斜 D. 银圈向下倾斜
【答案】C
【解析】
利用金属活动性顺序,结合化学方程式计算判断出铁圈和银圈的质量变化情况。
铁的金属活动性比铜强,铁能与硫酸铜溶液反应生成硫酸亚铁和铜,生成铜覆盖在铁的表面,根据化学方程式Fe+CuSO4=Cu+FeSO4可知,每56份质量的铁能置换出64份质量的铜,生成的铜的质量大于消耗的铁的质量,铁圈的质量增加;银的活动性比铜弱,不与硫酸铜溶液反应,银圈的质量不变;所以铁圈向下倾斜。故选C。

练习册系列答案
相关题目
【题目】下图是制取二氧化碳并进行有关物质的性质实验的装置。请根据要求回答有关问题。
查阅资料可知:氢氧化钠可以吸收二氧化碳,反应的方程式为:CO2+2NaOH=Na2CO3+H2O
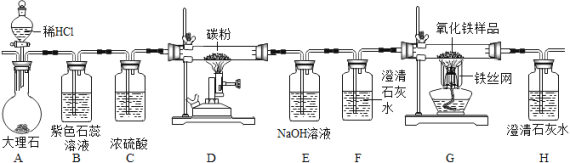
(1)写出下列装置中的化学方程式:装置A:______,装置G__________
(2)实验过程中装置B中的现象是_________装置F的作用是_______
(3)将A中的稀盐酸不断滴入大理石后,应先点燃_________(选填D或G处)的酒精灯。
(4)充分反应前后G装置的质量分别表示于右下表中,则样品中氧化铁的的质量为_____g
G | |
反应前(g) | 57.8 |
反应后(g) | 55.4 |
(5)该装置有一处明显的不足,请你给出改进的具体措施_________