题目内容
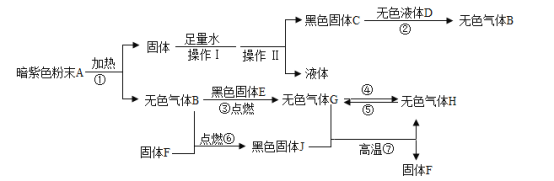
【题目】下列是初中部分常见物质的转换关系,已知,固体F是银白色的金属。C、D、G、H、J属于氧化物。请做出合理推断并完成下面的问题。
(1)写出固体F的化学式______,属于纯净物中的______类别。
(2)操作E名称为______,黑色固体C在反应②中的作用是______。
(3)反应③的基本反应类型是______。
(4)写出反应⑦的化学反应方程式是______,该反应体现了气体G具有______。
(5)反应①和反应②都可用于实验室制取无色气体B,同学们讨论后认为较好的方法是②,你觉得同学们的理由是:______。(写2条理由)
【答案】Fe 单质 过滤 催化作用 化合反应 4CO+Fe3O4![]() 3Fe+4CO2 还原性 不用加热,操作简单
3Fe+4CO2 还原性 不用加热,操作简单
【解析】
根据转换关系,固体F是银白色的金属,C、D、G、H、J属于氧化物,暗紫色粉末A加热会生成无色气体B,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,所以A是高锰酸钾,B是氧气,F和氧气点燃生成黑色固体J,所以F是铁,J是四氧化三铁,二氧化锰难溶于水,锰酸钾溶于水,所以C是二氧化锰,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,所以D是过氧化氢溶液,氧气和碳点燃生成一氧化碳,一氧化碳和四氧化三铁在高温的条件下生成铁和二氧化碳,所以G是一氧化碳,H是二氧化碳,经过验证,推导正确,
(1)经分析,可知固体F的化学式是Fe,属于纯净物中的单质类别;
(2)操作E可以将固体从溶液中分离出来,所以名称为过滤,黑色固体C在反应②中的作用是催化作用;
(3)反应③是碳和氧气在点燃的条件下生成一氧化碳,基本反应类型是化合反应;
(4)反应⑦是一氧化碳和四氧化三铁在高温的条件下生成铁和二氧化碳,化学方程式是:4CO+Fe3O4![]() 3Fe+4CO2,该反应体现了一氧化碳气体具有还原性;
3Fe+4CO2,该反应体现了一氧化碳气体具有还原性;
(5)反应①和反应②都可用于实验室制取无色气体氧气,同学们讨论后认为较好的方法是②,过氧化氢在二氧化锰催化作用下制取氧气,因为该反应不用加热,操作简单。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案