题目内容
 15、某化学课外兴趣小组,开展了以下两项活动:
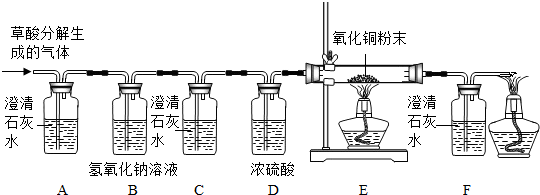
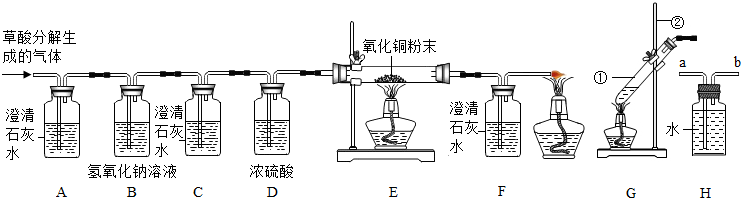
15、某化学课外兴趣小组,开展了以下两项活动:(1)第一组探究空气中氧气的含量.他们设计了如右图的装置,研究空气中所含氧气的体积,用一个50mL量筒倒扣在水中,使量筒内外液面均位于40mL处.量筒内浮着一个铜制的小船,船中放有足量白磷.现把浓硫酸缓缓倒入水中并搅拌.一会儿,白磷发生自燃,量筒内液面上升,向水槽内加水,至水槽与量筒内液面相平,读出读数.
①加入浓硫酸的的目的是
浓硫酸溶于水放热,使温度达到白磷的着火点以上
;②放白磷的小船用铜做的原因是
铜导热性好且化学性质稳定
;③最终,液面大约位于量筒刻度
32mL
处;④为何要向水槽内加水至内外液面相平
使气体内外压强相等,从而测得的气体体积更精确
;⑤试评价该兴趣小组的设计在选用仪器上有何缺陷
量筒不能用作反应容器
.(2)配制4%的氢氧化钠溶液200g,并用此溶液测定某硫酸溶液的溶质质量分数.
①配制200g质量分数为4%的氢氧化钠溶液,需要氢氧化钠固体的质量为
8
g,水的体积为192
mL(水的密度近似看作1g/cm3).②配制氢氧化钠溶液时,需要的玻璃仪器有量筒、烧杯、玻璃棒
及
胶头滴管
.配制好的氢氧化钠溶液要密封保存,其原因是:CO2+2NaOH=Na2CO3+H2O
(写化学方程式).③用配得的氢氧化钠溶液与待测溶质质量分数的硫酸溶液反应,
 实验过程中溶液的pH变化曲线如右图所示:
实验过程中溶液的pH变化曲线如右图所示:I、要得到此变化曲线,所进行的操作是
B
(填字母).A、将硫酸溶液滴加到氢氧化钠溶液中 B、将氢氧化钠溶液滴加到硫酸溶液中
II、b点对应的溶液中的溶质为
Na2SO4和NaOH
(写化学式).④恰好完全反应时,消耗20g氢氧化钠溶液和25g硫酸溶液,试计算该硫酸溶液中溶质的质量分数(请写出计算过程)
3.92%
.分析:(1)①白磷燃烧需要一定的温度②盛放白磷的容器要有很好的导热性③氧气被消耗,气体体积减小,压强减小④气体体积受压强影响大,读数时要保证压强内外相同⑤量筒不能用作反应容器
(2)①溶质质量=溶液质量×溶质质量分数 溶液质量=溶剂质量+溶质质量②配制溶液还要用到胶头滴管,NaOH在空气中能与CO2反应③I有图象可知溶液有酸性变为碱性IIb点溶液显碱性,硫酸全部反应,氢氧化钠有剩余④恰好完全反应说明,氢氧化钠和硫酸都没剩余
(2)①溶质质量=溶液质量×溶质质量分数 溶液质量=溶剂质量+溶质质量②配制溶液还要用到胶头滴管,NaOH在空气中能与CO2反应③I有图象可知溶液有酸性变为碱性IIb点溶液显碱性,硫酸全部反应,氢氧化钠有剩余④恰好完全反应说明,氢氧化钠和硫酸都没剩余
解答:解:(1)①白磷燃烧需要一定的温度,故加入浓硫酸的目的是:浓硫酸溶于水放热,使温度达到白磷的着火点以上
②盛放白磷的容器要有很好的导热性,故放白磷的小船用铜做的原因是:铜导热性好且化学性质稳定
③氧气被消耗,氧气体积占空气体积的五分之一,所以体积缩小8毫升,故液面大约位于量筒刻度32mL处.
④气体体积受压强影响大,读数时要保证压强内外相同,向水槽内加水至内外液面相平的目的为:使气体内外压强相等,从而测得的气体体积更精确
⑤量筒不能用作反应容器
(2)①溶质质量=溶液质量×溶质质量分数,故需要氢氧化钠固体的质量为:200g×4%=8g,溶液质量=溶剂质量+溶质质量,故需要水的质量为:200g-8g=192g需水的体积为192ml
②配制溶液还要用到胶头滴管,NaOH在空气中能与CO2反应,故氢氧化钠溶液要密封保存,其原因是:
CO2+2NaOH=Na2CO3+H2O
③I有图象可知溶液有酸性变为碱性,所进行的操作是将氢氧化钠溶液滴加到硫酸溶液中,故选B
II b点溶液显碱性,硫酸全部反应,氢氧化钠有剩余,故溶质为:Na2SO4和NaOH
④氢氧化钠的质量为:20g×4%=0.8g 设硫酸溶液的质量分数为x,则硫酸的质量为:25xg
2NaOH+H2SO4=Na2SO4+2H2O
80 98
0.8g 25xg
80/98=0.8g/25xg
x=3.92%
故:硫酸溶液的质量分数为3.92%
②盛放白磷的容器要有很好的导热性,故放白磷的小船用铜做的原因是:铜导热性好且化学性质稳定
③氧气被消耗,氧气体积占空气体积的五分之一,所以体积缩小8毫升,故液面大约位于量筒刻度32mL处.
④气体体积受压强影响大,读数时要保证压强内外相同,向水槽内加水至内外液面相平的目的为:使气体内外压强相等,从而测得的气体体积更精确
⑤量筒不能用作反应容器
(2)①溶质质量=溶液质量×溶质质量分数,故需要氢氧化钠固体的质量为:200g×4%=8g,溶液质量=溶剂质量+溶质质量,故需要水的质量为:200g-8g=192g需水的体积为192ml
②配制溶液还要用到胶头滴管,NaOH在空气中能与CO2反应,故氢氧化钠溶液要密封保存,其原因是:
CO2+2NaOH=Na2CO3+H2O
③I有图象可知溶液有酸性变为碱性,所进行的操作是将氢氧化钠溶液滴加到硫酸溶液中,故选B
II b点溶液显碱性,硫酸全部反应,氢氧化钠有剩余,故溶质为:Na2SO4和NaOH
④氢氧化钠的质量为:20g×4%=0.8g 设硫酸溶液的质量分数为x,则硫酸的质量为:25xg
2NaOH+H2SO4=Na2SO4+2H2O
80 98
0.8g 25xg
80/98=0.8g/25xg
x=3.92%
故:硫酸溶液的质量分数为3.92%
点评:(1)根据实验目的,理解实验操作
(2)根据图象理解表达的含义,进行相关计算
(2)根据图象理解表达的含义,进行相关计算

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某化学课外兴趣小组为探究Na与CO2的反应进行了如下实验(实验部分装置如图所示):向盛有Na的装置A中通入纯净、干燥的CO2,当观察到装置B中刚好出现浑浊时,点燃酒精灯,同时继续缓缓通入CO2,Na剧烈燃烧,产生白烟,燃烧结束后装置A中有黑色固体和白色固体生成.

资料卡:
(1)K、Ca、Na等活泼金属的氧化物均可与水反应生成对应的碱;
(2)钠为银白色金属,过氧化钠为淡黄色固体.
(一)提出问题:白色固体含有什么物质?
(二)猜想与假设:
假设1:白色固体含有 ;
假设2:白色固体含有Na2O;
(三)实验设计:
(四)反思提高:
Na在CO2中燃烧存在多个反应、生成多种物质.请你写出其中生成物仅为一种白色固体与一种黑色固体的反应的化学方程式: .

资料卡:
(1)K、Ca、Na等活泼金属的氧化物均可与水反应生成对应的碱;
(2)钠为银白色金属,过氧化钠为淡黄色固体.
(一)提出问题:白色固体含有什么物质?
(二)猜想与假设:
假设1:白色固体含有
假设2:白色固体含有Na2O;
(三)实验设计:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量白色固体放入足量水中 | 白色固体完全溶解 | |
| ②取①中少量溶液,加入 |
产生大量气泡 | 假设1成立 |
| ③另取①中少量溶液, |
假设2成立 |
Na在CO2中燃烧存在多个反应、生成多种物质.请你写出其中生成物仅为一种白色固体与一种黑色固体的反应的化学方程式: