题目内容
(2010?大兴区二模)50g镁、锌、铁的混合物与足量的稀硫酸反应得到混合溶液,蒸发后得到218g固体(已换算成无水硫酸盐).则反应产生氢气的质量是( )
【答案】分析:已知Mg→MgSO4; Zn→ZnSO4; Fe→FeSO4.并且可知道,这个变化中,增加的质量是硫酸根的质量218g-50g=168g,在H2SO4中 氢元素与硫酸根的质量比为2:96.
解答:解:设生成氢气的质量为x,根据关系式A→ASO4→SO4→H2↑,
则2:96=x:168g
x=3.5g;故选C.
点评:运用质量守恒定律,了解物质反应前后有什么不同,从中找出规律
解答:解:设生成氢气的质量为x,根据关系式A→ASO4→SO4→H2↑,
则2:96=x:168g
x=3.5g;故选C.
点评:运用质量守恒定律,了解物质反应前后有什么不同,从中找出规律

练习册系列答案
相关题目
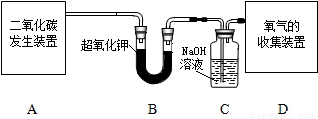
(2010?大兴区二模)人呼出的气体中含有的水分也能与超氧化钾反应生成氧气.
[作出猜想]二氧化碳与超氧化钾反应生成的化合物到底是哪种物质?
甲同学作出了以下三种猜想:①是一种酸; ②是一种碱; ③是一种碳酸盐.
(1)通过对反应物有关的元素组成的分析,乙同学认为猜想______(填数字序号)一定是错误的,理由是______.
(2)[进行实验]同学们通过以下实验验证了甲同学的另一个猜想是正确的,请完成下述实验报告.
(3)简述鉴定氧自救器药罐中生氧剂超氧化钾是否需要更换的简便的化学方法______.
[作出猜想]二氧化碳与超氧化钾反应生成的化合物到底是哪种物质?
甲同学作出了以下三种猜想:①是一种酸; ②是一种碱; ③是一种碳酸盐.
(1)通过对反应物有关的元素组成的分析,乙同学认为猜想______(填数字序号)一定是错误的,理由是______.
(2)[进行实验]同学们通过以下实验验证了甲同学的另一个猜想是正确的,请完成下述实验报告.
| 实验步骤 | 实验现象 | 实验结论 |