题目内容
【题目】一包白色固体中可能含有碳酸钠、硫酸钠、氯化钾、硝酸钡、氢氧化钠中的一种或几种.某小组为探究其成分进行如下实验:
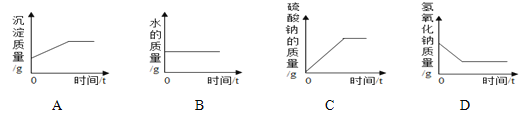
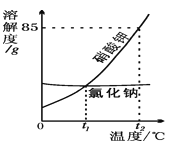
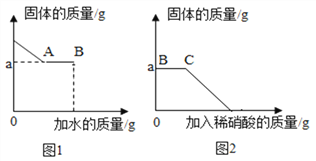
Ⅰ.取少量固体于烧杯中逐渐加水并不断搅拌,烧杯中固体质量随加入的水的质量变化如图1
Ⅱ.取少量B点时的清液于试管中,滴加酚酞溶液,酚酞变红
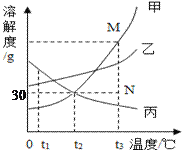
Ⅲ.向实验Ⅰ所得的混合物中滴加稀硝酸并不断搅拌,烧杯内固体的质量随加入稀硝酸的质量的变化如图2所示.
下列分析错误的是( )
A. 由实验Ⅱ说明溶液pH>7
B. 由实验Ⅱ、Ⅲ说明该白色固体中一定含有Na2CO3、Ba(NO3)2、NaOH
C. B点时的清液中一定含Na+、NO3-
D. 若取实验Ⅲ后的溶液于试管中,加入AgNO3溶液,产生白色沉淀,则存在KCl
【答案】C
【解析】由图1可知,加入水,有不溶物,说明了上述物质间发生反应生成了沉淀,由于碳酸钠、硫酸钠都能与硝酸钡反应生成沉淀,由此可知,一定存在硝酸钡;由图2可知沉淀加入一定量的稀硝酸后,沉淀全部溶解,说明溶液中有物质先与硝酸发生反应,将该物质反应完后再与沉淀反应,故沉淀应为碳酸钡,说明了原混合物中一定有碳酸钠;又由取少量B点时的清液于试管中,滴加酚酞溶液,酚酞变红,说明于硝酸反应的是氢氧化钠。A、由实验Ⅱ取少量B点时的清液于试管中,滴加酚酞溶液,酚酞变红,说明溶液pH>7,正确;B、由上述分析可知,原白色固体中一定含有Na2CO3、Ba(NO3)2、NaOH,正确;C、由B可知,B点时的清液中一定含Na+、NO3-、OH-,错误;D、由于银离子与氯离子不能共存,若取实验Ⅲ后的溶液于试管中,加入AgNO3溶液,产生白色沉淀,则存在KCl,正确。故选C。

练习册系列答案
相关题目