题目内容
(2004?防城港)有4瓶无色溶液A、B、C、D分别是盐酸、氢氧化钠、氯化钠和硝酸钾溶液中的一种,实验过程及反应现象如下图所示: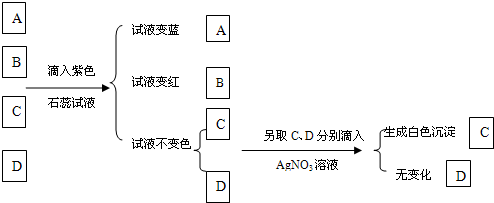
(1)说明A、B、C、D分别是什么溶液:
A为
(2)写出生成白色沉淀的化学反应方程式.

(1)说明A、B、C、D分别是什么溶液:
A为
NaOH(或氢氧化钠)
NaOH(或氢氧化钠)
,B为HCl(或盐酸)
HCl(或盐酸)
,C为NaCl(或氯化钠)
NaCl(或氯化钠)
,D为KNO3(或硝酸钾)
KNO3(或硝酸钾)
;(2)写出生成白色沉淀的化学反应方程式.
NaCl+AgNO3=AgCl↓+NaNO3
NaCl+AgNO3=AgCl↓+NaNO3
.分析:(1)根据紫色石蕊试液遇酸变红色,遇碱变蓝色,盐酸溶液为酸溶液,氢氧化钠溶液为碱溶液,氯化钠和硝酸钾溶液为中性溶液,则可推出A和B,然后利用C、D与硝酸银溶液反应,C有白色沉淀生成,确定C,另一物质为D;
(2)生成白色沉淀的反应为氯化钠与硝酸银的反应,然后书写化学反应方程式.
(2)生成白色沉淀的反应为氯化钠与硝酸银的反应,然后书写化学反应方程式.
解答:解:(1)因盐酸溶液为酸溶液,氢氧化钠溶液为碱溶液,氯化钠和硝酸钾溶液为中性溶液,且紫色石蕊试液遇酸变红色,遇碱变蓝色,则A为氢氧化钠,B为盐酸,再由C、D与硝酸银溶液反应,可知C为白色沉淀生成,则C为氯化钠,则D为硝酸钾,故答案为:NaOH(或氢氧化钠);HCl(或盐酸);NaCl (或氯化钠);KNO3 (或硝酸钾);
(2)因氯化钠与硝酸银反应生成氯化银沉淀和硝酸钠,则反应为NaCl+AgNO3=AgCl↓+NaNO3,
故答案为:NaCl+AgNO3=AgCl↓+NaNO3.
(2)因氯化钠与硝酸银反应生成氯化银沉淀和硝酸钠,则反应为NaCl+AgNO3=AgCl↓+NaNO3,
故答案为:NaCl+AgNO3=AgCl↓+NaNO3.
点评:本题考查利用物质的性质来推断酸、碱、盐,学生应熟悉酸、碱、盐的性质及常见的复分解反应来分析解答.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目