题目内容
 甲乙两种固体的溶解度曲线如图.下列说法中正确的是( )
甲乙两种固体的溶解度曲线如图.下列说法中正确的是( )分析:A、比较溶解度大小须确定温度;
B、据该温度下二者的溶解度及溶质的质量分数计算方法解答;
C、据甲、乙的溶解度随温度变化情况及40℃时,甲、乙的溶解度分析解答;
D、饱和溶液中溶质的质量分数的计算式
×100%,结合二者的溶解度分析解答.
B、据该温度下二者的溶解度及溶质的质量分数计算方法解答;
C、据甲、乙的溶解度随温度变化情况及40℃时,甲、乙的溶解度分析解答;
D、饱和溶液中溶质的质量分数的计算式
| 溶解度 |
| 溶解度+100g |
解答:解:A、比较溶解度大小须确定温度,故描述 错误;
B、40℃时,甲、乙的溶解度分别是50g、40g,所以40℃时,分别在100g水中加入50g甲、乙,乙不能完全溶解,故所得溶液中溶质的质量分数不相等,故错误;
C、20℃时甲乙二者的溶解度相等,均为30g,所以分别在100g水中加入50g甲、乙,形成的是饱和溶液,加热到40℃时,甲的溶解度变为50g,乙的溶解度变为40g,甲恰好饱和,乙溶液也是饱和溶液,故正确;
D、20℃时甲乙二者的溶解度相等,均为30g,二者的溶质质量分数是:
×100%<30%,故错误;
故选:C.
B、40℃时,甲、乙的溶解度分别是50g、40g,所以40℃时,分别在100g水中加入50g甲、乙,乙不能完全溶解,故所得溶液中溶质的质量分数不相等,故错误;
C、20℃时甲乙二者的溶解度相等,均为30g,所以分别在100g水中加入50g甲、乙,形成的是饱和溶液,加热到40℃时,甲的溶解度变为50g,乙的溶解度变为40g,甲恰好饱和,乙溶液也是饱和溶液,故正确;
D、20℃时甲乙二者的溶解度相等,均为30g,二者的溶质质量分数是:
| 30g |
| 130g |
故选:C.
点评:了解溶解度概念、溶质的质量分数、溶解度曲线的意义等知识并会灵活应用,考查了学生分析、解决问题的能力.

练习册系列答案
相关题目
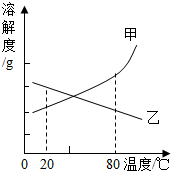 (2013?许昌二模)甲乙两种固体的溶解度曲线如图所示,现有80℃时两者的饱和溶液各半烧杯,且烧杯中均含有少量甲和乙固体.现将温度从80℃降到20℃,下列说法正确的是( )
(2013?许昌二模)甲乙两种固体的溶解度曲线如图所示,现有80℃时两者的饱和溶液各半烧杯,且烧杯中均含有少量甲和乙固体.现将温度从80℃降到20℃,下列说法正确的是( )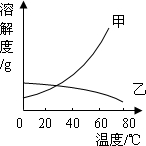 (2012?沐川县二模)甲乙两种固体的溶解度曲线如图所示.有一个大烧杯中装着含有甲和乙的两种饱和溶液,而且杯中还有少量甲和乙的固体存在.现将温度由80℃降到20℃.下列说法错误的是( )
(2012?沐川县二模)甲乙两种固体的溶解度曲线如图所示.有一个大烧杯中装着含有甲和乙的两种饱和溶液,而且杯中还有少量甲和乙的固体存在.现将温度由80℃降到20℃.下列说法错误的是( )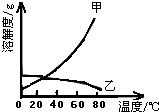 甲乙两种固体的溶解度曲线如图所示.有一个大烧杯中装着含有甲和乙的两种饱和溶液,而且杯中还有少量甲和乙的固体存在.现将温度由80℃降到20℃.下列说法错误的是 ( )
甲乙两种固体的溶解度曲线如图所示.有一个大烧杯中装着含有甲和乙的两种饱和溶液,而且杯中还有少量甲和乙的固体存在.现将温度由80℃降到20℃.下列说法错误的是 ( )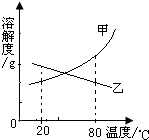 甲乙两种固体的溶解度曲线如图所示.现有80℃时两者的饱和溶液各半烧杯,且烧杯中均含有少量甲和乙固体.现将温度从80℃降到20℃,下列说法正确的是( )
甲乙两种固体的溶解度曲线如图所示.现有80℃时两者的饱和溶液各半烧杯,且烧杯中均含有少量甲和乙固体.现将温度从80℃降到20℃,下列说法正确的是( )