题目内容
R元素的一个原子质量是一个碳原子质量的12倍,则一个R原子的质量约为一个氧原子质量的( )
| A、8倍 | B、9倍 | C、16倍 | D、18倍 |
分析:根据题意并结合碳、氧原子的原子质量即可作答.
解答:解:从元素周期表可知:碳原子的相对原子质量为12、氧原子的相对原子质量为16,而R元素的一个原子质量是一个碳原子质量的12倍,
则有一个R原子的相对原子质量=12×12=144,
所以有一个R原子的质量约为一个氧原子质量的
=9倍,
故选B.
则有一个R原子的相对原子质量=12×12=144,
所以有一个R原子的质量约为一个氧原子质量的
| 144 |
| 16 |
故选B.
点评:本题考查了相对原子质量的计算方法,常见元素的相对原子质量需要同学们了解.

练习册系列答案
 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
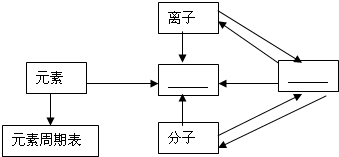 构建知识网络是一种重要的学习方法.某同学对物质组成和结构方面的知识进行了归纳,请填写空白,完成设计.
构建知识网络是一种重要的学习方法.某同学对物质组成和结构方面的知识进行了归纳,请填写空白,完成设计.