题目内容
【题目】化学是造福人类的科学.请利用所学知识回答下列问题.
I.化学帮助我们正确认识物质
(1)氧气可用于_______(填一种用途),但氧气也是导致铁锈蚀的因素之一.写出防止铁生锈的一种方法:__________.
Ⅱ.化学指导人类合理利用资源
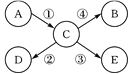
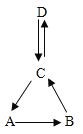
(2)如图是化学家研究出的高效、经济的制氢途径.
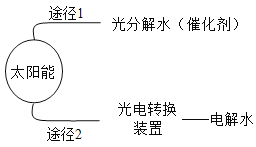
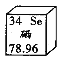
途径1:常用二氧化钛(TiO2)作催化剂.二氧化钛中钛元素的化合价为_____.
途径2:电解水是将电能转化为_____能.
Ⅲ.化学促进科学技术的发展
(3)科学家研制出有“自我修复能力”的塑料.塑料属于__________(选填“无机”、“合成”或“复合”)材料.
(4)二氧化硅(SiO2)可用于制造光导纤维.氧气和四氯化硅蒸气(SiCl4)在高温条件下可反应生成二氧化硅和氯气(Cl2),该反应的化学方程式是_____________.
【答案】冶炼钢铁 涂油 +4 化学 合成 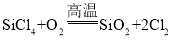
【解析】
金属生锈是金属和水和氧气共同作用的结果,化合物中正负化合价的代数和为零,电解水是将电能转化为化学能。
(1)氧气可用于冶炼钢铁、急救病人等;金属生锈是金属和水和氧气共同作用的结果,常见的防止铁生锈的方法有涂油、喷漆、烤蓝、搪瓷等。
(2)途径1:在TiO2中氧的化合价为﹣2价,根据化合物中正负化合价的代数和为零,设钛元素的化合价为x,![]() ,x=+4,则二氧化钛中钛元素的化合价为+4。
,x=+4,则二氧化钛中钛元素的化合价为+4。
途径2:水电解生成氢气和氧气,故电解水是将电能转化为化学能。
(3)有机合成材料包括合成纤维、合成橡胶和塑料,故塑料属于有机合成材料。
(4)反应物是氧气和四氯化硅蒸气(SiCl4),反应是在高温条件下,生成物是二氧化硅和氯气(Cl2),反应的化学方程式是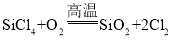 。
。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案【题目】下列表中的叙述、对应的化学方程式和所属反应类型都正确的是( )
选项 | 叙述 | 化学反应方程式 | 反应类型 |
A | 拉瓦锡研究空气成分 | 2HgO | 分解反应 |
B | 探究一氧化碳的还原性 | CO+CuO | 置换反应 |
C | 用二氧化碳制作碳酸饮料 | CO2+H2O═H2CO3 | 化和反应 |
D | 服用含氢氧化铝的药物治疗胃酸过多 | Al(OH)3+3HCl═AlCl3+3H2O | 复分解反应 |
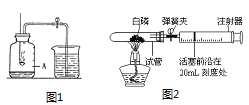
【题目】在高温下,铁与水蒸气能发生反应生成一种常见铁的氧化物和一种气体,某化学 学习小组的同学对此反应甩感兴趣,在小组集体协作下设计了如下实验,以探究铁粉与水蒸气反应后的产物,也邀请你一起来完成下列探究:
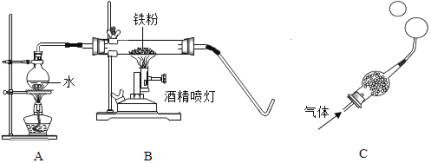
(1)A装置的作用是___;
(2)探究生成的气体是什么?
(猜想与假设)猜想一:生成的气体可能是氢气;
猜想二:生成的气体可能是氧气;
(实验探究)将生成的气体通入C装置,球形管里装有碱石灰干燥剂,导管口蘸些肥皂水(或洗涤剂溶液),控制气体流速,吹出肥皂泡,当肥皂泡吹到一定大时,轻轻摆动导管,肥皂泡脱离管口后,气泡上升.用燃着的木条靠近肥皂泡,有爆鸣声.
(推断)生成的气体是___.
(3)探究试管中剩余固体成分是什么?
(查阅资料)
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被进磁铁吸引 | 否 | 否 | 能 |
能否与盐酸反应 | 能 | 能 | 能 |
(初步验证)试管中剩余固体为黑色,能全部被磁铁吸引.
(猜想与假设)猜想一:剩余固体是Fe和Fe3O4;
猜想二:剩余固体是:___.
(实验探究)
实验操作 | 实验现象及结论 |
____ | _____ |
[实检结论]铁与水蒸气反应的化学方程式为:___.
(反思与交流)该黑色固体不可能是FeO、Fe2O3,理由是___.