题目内容
【题目】如图是A、B、C、D四种粒子的结构示意图,回答下列问题: 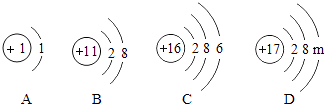
(1)A、B、C属于离子的是(填写离子符号).
(2)若D表示某元素原子,则m= , 该元素的原子在化学反应中容易(选填“得到”或“失去”)电子.
(3)在A、C形成的化合物中,C元素的化合价为 .
【答案】
(1)Na+
(2)7;得到
(3)﹣2
【解析】解:(1)决定元素的化学性质的是原子的最外层电子数,故A、B、C属于离子的是B,其为 Na+;(2)根据原子核内质子数=电子数,则17=m+2+8,则m=7.为非金属元素,故该元素的原子在化学反应中容易得到电子;(3)根据决定元素种类的是核电荷数(即核内质子数),则A为氢元素,C为硫元素,且C最外层电子数均为6,易得2个电子,A、C形成的化合物为H2S,因为氢元素的化合价为+1,故C元素的化合价为﹣2价. 所以答案是:(1)Na+;(2)7; 得到;(3)﹣2.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目