题目内容
(2010?济南)如图在托盘天平两边各放一只烧杯,调节至平衡.往右边烧杯里注入一定量的稀硫酸,左边烧杯里注入相同质量的盐酸.
(1).两边烧杯里各投入少量相同质量的锌粒,锌粒完全溶解后,天平指针有何变化?.为什么?.
(2).左边投入少许锌粒,右边投入相同质量的镁条,锌、镁完全溶解后,天平指针有何变化..为什么?.
【答案】分析:反应物放在一起不反应的状态时,天平是平衡的,指针的偏转主要是看生成氢气的多少,因此解题时判断氢气多少则成为解题的关键所在.
解答:解:(1)相同质量的锌粒,锌粒都完全溶解,应根据金属锌的质量进行计算;
此题中虽没有说明反应时金属的质量,根据化学方程式
Zn+H2SO4═ZnSO4+H2↑
65 2
Zn+2HCl═ZnCl2+H2↑
65 2
由于同质量的锌反应生成的氢气相等,故反应后天平保持平衡;
(2)锌粒和镁条全部溶解,说明酸足量,设金属的质量为65,镁生成的氢气质量为y
Zn+2HCl═ZnCl2+H2↑
65 2
Mg+H2SO4═MgSO4+H2↑
24 2
65 y
y=5.4
镁生成的氢气多,指针偏左.
故答案为:(1)指针不偏转,生成的氢气量相等;(2)指针偏左,镁生成的氢气多.
点评:本题考查了金属与酸反应生成氢气质量的关系,完成此题,可以依据反应的化学方程式,从酸的质量和金属的质量的角度进行.
解答:解:(1)相同质量的锌粒,锌粒都完全溶解,应根据金属锌的质量进行计算;
此题中虽没有说明反应时金属的质量,根据化学方程式
Zn+H2SO4═ZnSO4+H2↑
65 2
Zn+2HCl═ZnCl2+H2↑
65 2
由于同质量的锌反应生成的氢气相等,故反应后天平保持平衡;
(2)锌粒和镁条全部溶解,说明酸足量,设金属的质量为65,镁生成的氢气质量为y
Zn+2HCl═ZnCl2+H2↑
65 2
Mg+H2SO4═MgSO4+H2↑
24 2
65 y
y=5.4
镁生成的氢气多,指针偏左.
故答案为:(1)指针不偏转,生成的氢气量相等;(2)指针偏左,镁生成的氢气多.
点评:本题考查了金属与酸反应生成氢气质量的关系,完成此题,可以依据反应的化学方程式,从酸的质量和金属的质量的角度进行.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目

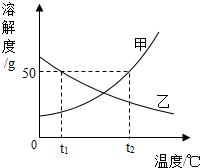 (2010?济南)如图是甲、乙两种不含结晶水的固体物质的溶解度曲线.根据图示判断,下列有关说法中,错误的是( )
(2010?济南)如图是甲、乙两种不含结晶水的固体物质的溶解度曲线.根据图示判断,下列有关说法中,错误的是( )