题目内容
(2012?平顶山一模)相同质量的KClO3、H2O2和H2O,完全分解产生氧气的质量( )
分析:首先比较KClO3和H2O,因为它们化学式中的氧元素全部转化为氧气.根据相同质量的氧元素,物质质量越少的,在物质质量相同的情况下,则生成的氧气越多进行比较,然后选出放出氧气质量最多的再与双氧水比较,双氧水中有一半的氧元素转化为氧气.
解答:解:KClO3和H2O中的氧元素全部转化为氧气,可通过比较相同质量的氧元素,物质质量越少的,在物质质量相同的情况下,则生成的氧气越多,故化学式可改为:KClO3和H6O3,很显然,是水分解产生的氧气多.
再比较水和双氧水,双氧水中有一半的氧元素转化为氧气,故H2O2和H2O分子个数一样多时,放出的氧气质量相等,由分子可以看出,当质量相等时,水放出的氧气质量最多.
故选C
再比较水和双氧水,双氧水中有一半的氧元素转化为氧气,故H2O2和H2O分子个数一样多时,放出的氧气质量相等,由分子可以看出,当质量相等时,水放出的氧气质量最多.
故选C
点评:解答本题可利用质量守恒定律元素守恒进行相关分析计算,只有这样才能对问题做出正确的判断.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
 (2012?平顶山一模)下图是用来表示物质间发生化学变化的模型示意图,图中“
(2012?平顶山一模)下图是用来表示物质间发生化学变化的模型示意图,图中“ 、
、 ”分别表示两种不同元素的原子.能用该示意图表示的反应是( )
”分别表示两种不同元素的原子.能用该示意图表示的反应是( )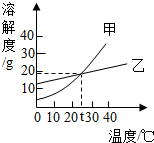 (2012?平顶山一模)如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )
(2012?平顶山一模)如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )