题目内容
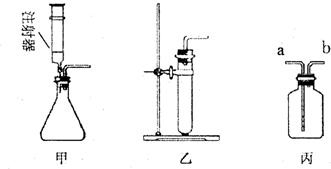
“用双氧水和二氧化锰制氧气”的反应方程式为________.某研究小组对用H2O2分解生成H2O和O2的实验条件进行探究.他们进行了实验:
| 编号 | 实验 | 现象 |
| ① | 往盛有5 mL 5% H2O2溶液的试管中,伸入带火星的木条, | 木条不复燃 |
| ② | 往盛有5 mL 5% H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条, | 木条复燃 |
(1)设计实验①的目的是________.
(2)如果要证明MnO2是否是上述反应的催化剂,还需要检验________.
研究小组还展开了催化剂MnO2的用量对反应速率有没有影响的思考与探究:
他做了这样一组实验:每次均用30mL 10%的H2O2溶液,采用不同量MnO2粉末作催化剂,测定各次收集到500mL氧气时所用的时间,结果如表(其他实验条件均相同):
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| MnO2粉末用量(g) | O.1 | 0.2 | 0.3 | 0.4 | 0.5 | O.6 | 0.7 | 0.8 | O.9 | 1.O |
| 所用时间(s) | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 | 2 | 2 |
(3)请分析表中数据回答:MnO2的用量对反应速率有没有影响?如果有,是怎样影响的呢?答:________.
解:根据实验室用双氧水和二氧化锰制氧气反应原理,反应方程式为:2H2O2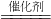 2H2O+O2↑;故答案为:2H2O2
2H2O+O2↑;故答案为:2H2O2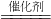 2H2O+O2↑;
2H2O+O2↑;
(1)根据观察常温下双氧水能否分解产生氧气,和实验2作比较;
故答案为:观察常温下双氧水能否分解出氧产生氧气,以便于MnO2对双氧水的作用的比较;
(2)根据催化剂在反应前后质量和化学性质都没有发生变化的性质可知:要证明MnO2是否是上述反应的催化剂,还需要检验:反应后MnO2的质量;
故答案为:反应后MnO2的质量;
(3)根据实验所提供的数据进行观察发现其特点:当双氧水用量一定时,随着二氧化锰粉末用量的增加,所收集到氧气的时间越来越短;当达到一个定值后(0.7g)时间就变化不大了;
故答案为:MnO2的用量对反应速率有影响.在一定的用量范围内,MnO2用量的增加,反应所需的时间减少,反应速率增大;当MnO2的用量增加到一定的值后,继续增大MnO2的用量,反应速率不再增大.
分析:根据实验室用双氧水和二氧化锰制氧气反应原理,写出反应方程式解答;
(1)根据观察的实验现象做比较,观察常温下双氧水能否分解产生氧气,和实验2作比较,进行解答;
(2)根据在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质叫做催化剂,进行解答;
(3)根据实验所提供的数据进行观察发现其特点:当双氧水用量一定时,随着二氧化锰粉末用量的增加,所收集到氧气的时间越来越短;当达到一个定值后(0.7g)时间就变化不大了,进行分析解答本题.
点评:本题主要考查学生对实验室用双氧水和二氧化锰制氧气反应原理,及催化剂的应用的理解与掌握,观察实验数据分析探究的结果.
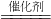 2H2O+O2↑;故答案为:2H2O2
2H2O+O2↑;故答案为:2H2O2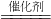 2H2O+O2↑;
2H2O+O2↑;(1)根据观察常温下双氧水能否分解产生氧气,和实验2作比较;
故答案为:观察常温下双氧水能否分解出氧产生氧气,以便于MnO2对双氧水的作用的比较;
(2)根据催化剂在反应前后质量和化学性质都没有发生变化的性质可知:要证明MnO2是否是上述反应的催化剂,还需要检验:反应后MnO2的质量;
故答案为:反应后MnO2的质量;
(3)根据实验所提供的数据进行观察发现其特点:当双氧水用量一定时,随着二氧化锰粉末用量的增加,所收集到氧气的时间越来越短;当达到一个定值后(0.7g)时间就变化不大了;
故答案为:MnO2的用量对反应速率有影响.在一定的用量范围内,MnO2用量的增加,反应所需的时间减少,反应速率增大;当MnO2的用量增加到一定的值后,继续增大MnO2的用量,反应速率不再增大.
分析:根据实验室用双氧水和二氧化锰制氧气反应原理,写出反应方程式解答;
(1)根据观察的实验现象做比较,观察常温下双氧水能否分解产生氧气,和实验2作比较,进行解答;
(2)根据在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质叫做催化剂,进行解答;
(3)根据实验所提供的数据进行观察发现其特点:当双氧水用量一定时,随着二氧化锰粉末用量的增加,所收集到氧气的时间越来越短;当达到一个定值后(0.7g)时间就变化不大了,进行分析解答本题.
点评:本题主要考查学生对实验室用双氧水和二氧化锰制氧气反应原理,及催化剂的应用的理解与掌握,观察实验数据分析探究的结果.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目