题目内容
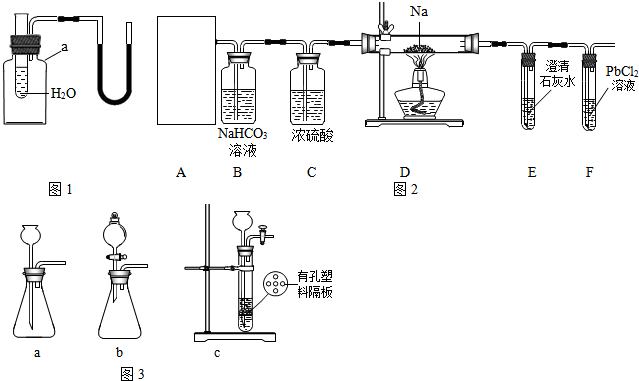
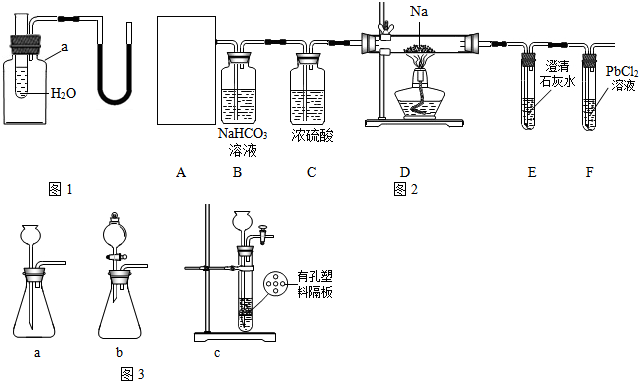
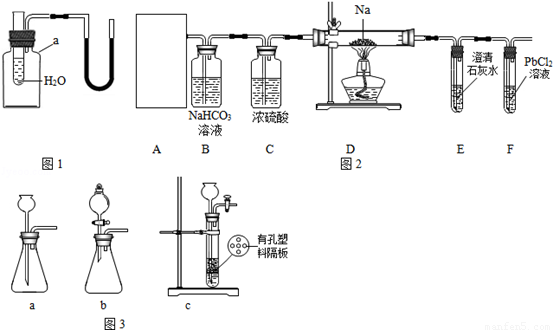
(1)用如图1所示装置进行实验,探究物质溶解是吸热还是放热,仪器a的名称是______.若出现导管中红墨水液面左管降低右管升高,则试管中加入的物质可以是______(填序号).
A.NH4NO3固体;B.浓硫酸;C.NaOH固体;D.CaCO3固体.
(2)实验室用氯酸钾和二氧化锰制氧气,反应的化学方程式是______,反应中二氧化锰的作用是______.要从充分反应后的剩余固体中分离出氯化钾晶体,需要进行的实验操作有______.
(3)某化学学习小组的同学在网上查资料时得知,金属钠着火不能用CO2灭火.他们想知道,Na与CO2反应究寓会生成什么物质呢?
【提出猜想】
Ⅰ.4Na+CO2 2Na2O+C
2Na2O+C
Ⅱ.4Na+3CO2 2Na2CO3+C
2Na2CO3+C
III.2Na+2CO2 Na2O+2CO
Na2O+2CO
溶液检验:PdCl2+CO+H2O═Pd(黑色)↓+2HCl+CO2
【实验操究】该小组成员设计了如图2所示实验:
【分析讨论】
①装置A用盐酸与石灰石反应制备CO2,反应的化学方程式为______.为使制备CO2的反应能随开随用,随关随停,所选装置应是图3中的______.
②装置B的作用是除去二氧化碳气体中混有的HCl气体,反应的化学方程式是______;装置C的作用是______.
③经检查整套装置气密性良好,装好药品使A中产生CO2,必须待装置E中出现______现象时再点燃酒精灯,其目的是______.
【实验结论】
实验观察到的现象是:装置D中的硬质玻璃管内残留白色固体,装置F中产生黑色沉淀,则猜想______是正确的.
解:(1)仪器a的名称是广口瓶;导管中红墨水液面左管降低右管升高,则试管中加入的物质溶于水时放热,NH4NO3固体溶于水时吸热;浓硫酸溶于水时放热;NaOH固体溶于水时放热;CaCO3固体不溶于水;
(2)实验室用氯酸钾和二氧化锰制氧气,反应的化学方程式是2KCl03 2KCl+3O2↑;反应中二氧化锰的作用是做催化剂;要从充分反应后的剩余固体中分离出氯化钾晶体,需要进行的实验操作有溶解、过滤、蒸发;
2KCl+3O2↑;反应中二氧化锰的作用是做催化剂;要从充分反应后的剩余固体中分离出氯化钾晶体,需要进行的实验操作有溶解、过滤、蒸发;
(3)【分析讨论】
①盐酸与石灰石反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;为使制备CO2的反应能随开随用,随关随停,所选装置应是图3中的c.
②碳酸氢钠和氯化氢反应生成氯化钠、水和二氧化碳,反应的化学方程式是HCl+NaHCO3═NaCl+H2O+CO2↑;浓硫酸具有吸水性,能除去二氧化碳气体中的水蒸气;
③为防止钠与氧气反应,因此应先排出反应装置中的空气,当装置E中澄清石灰水变浑浊时,说明空气已排除完毕;
【实验结论】
根据题中信息可知,若装置D中的硬质玻璃管内残留白色固体,装置F中产生黑色沉淀,则猜想Ⅲ正确;
故答案为:(1)广口瓶; BC;
(2)2KClO3 2KCl+3O2↑;作催化剂;溶解、过滤、蒸发;
2KCl+3O2↑;作催化剂;溶解、过滤、蒸发;
(3)【分析讨论】
①CaCO3+2HCl═CaCl2+H2O+CO2↑;c;
②HCl+NaHCO3═NaCl+H2O+CO2↑;除去二氧化碳气体中的水蒸气;
③澄清石灰水变浑浊;排出反应装置中的空气,防止钠与氧气反应;
【实验结论】根据实验观察到的现象是:装置D中的硬质玻璃管内残留白色固体,装置F中产生黑色沉淀,说明猜想Ⅲ是正确的;
故答案为:Ⅲ.
分析:(1)根据常见仪器的名称回答;导管中红墨水液面左管降低右管升高,则试管中加入的物质溶于水时放热;
(2)根据化学方程式书写的步骤写出氯酸钾和二氧化锰混合制取氧气的化学方程式即可;要从充分反应后的剩余固体中分离出氯化钾晶体,需要进行的实验操作有溶解、过滤、蒸发;
(3)【分析讨论】根据化学方程式的书写方法和各装置的作用进行分析;
【实验结论】根据题中信息结合实验现象进行分析.
点评:确理解实验装置的作用,为明确实验操作和实验目的基础和前提,难度较大.
(2)实验室用氯酸钾和二氧化锰制氧气,反应的化学方程式是2KCl03
 2KCl+3O2↑;反应中二氧化锰的作用是做催化剂;要从充分反应后的剩余固体中分离出氯化钾晶体,需要进行的实验操作有溶解、过滤、蒸发;
2KCl+3O2↑;反应中二氧化锰的作用是做催化剂;要从充分反应后的剩余固体中分离出氯化钾晶体,需要进行的实验操作有溶解、过滤、蒸发;(3)【分析讨论】
①盐酸与石灰石反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;为使制备CO2的反应能随开随用,随关随停,所选装置应是图3中的c.
②碳酸氢钠和氯化氢反应生成氯化钠、水和二氧化碳,反应的化学方程式是HCl+NaHCO3═NaCl+H2O+CO2↑;浓硫酸具有吸水性,能除去二氧化碳气体中的水蒸气;
③为防止钠与氧气反应,因此应先排出反应装置中的空气,当装置E中澄清石灰水变浑浊时,说明空气已排除完毕;
【实验结论】
根据题中信息可知,若装置D中的硬质玻璃管内残留白色固体,装置F中产生黑色沉淀,则猜想Ⅲ正确;
故答案为:(1)广口瓶; BC;
(2)2KClO3
 2KCl+3O2↑;作催化剂;溶解、过滤、蒸发;
2KCl+3O2↑;作催化剂;溶解、过滤、蒸发;(3)【分析讨论】
①CaCO3+2HCl═CaCl2+H2O+CO2↑;c;
②HCl+NaHCO3═NaCl+H2O+CO2↑;除去二氧化碳气体中的水蒸气;
③澄清石灰水变浑浊;排出反应装置中的空气,防止钠与氧气反应;
【实验结论】根据实验观察到的现象是:装置D中的硬质玻璃管内残留白色固体,装置F中产生黑色沉淀,说明猜想Ⅲ是正确的;
故答案为:Ⅲ.
分析:(1)根据常见仪器的名称回答;导管中红墨水液面左管降低右管升高,则试管中加入的物质溶于水时放热;
(2)根据化学方程式书写的步骤写出氯酸钾和二氧化锰混合制取氧气的化学方程式即可;要从充分反应后的剩余固体中分离出氯化钾晶体,需要进行的实验操作有溶解、过滤、蒸发;
(3)【分析讨论】根据化学方程式的书写方法和各装置的作用进行分析;
【实验结论】根据题中信息结合实验现象进行分析.
点评:确理解实验装置的作用,为明确实验操作和实验目的基础和前提,难度较大.

练习册系列答案
相关题目
 2Na2O+C
2Na2O+C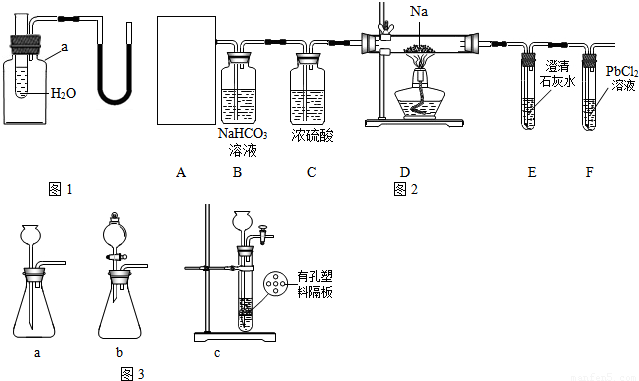
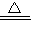 2Na2O+C
2Na2O+C 2Na2C03+C
2Na2C03+C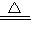 Na2O+2CO
Na2O+2CO