题目内容
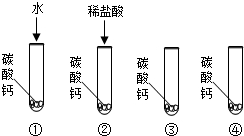 某同学通过实验来探究盐酸中哪种粒子(H2O、H+、Cl-)能使碳酸钙溶解并产生无色气体.请根据如图实验回答问题
某同学通过实验来探究盐酸中哪种粒子(H2O、H+、Cl-)能使碳酸钙溶解并产生无色气体.请根据如图实验回答问题(1)通过实验①可以证明
(2)要证明另外两种粒子能否溶解碳酸钙溶解,并产生无色气体,在③中应加入的物质是
(4)探究的结论是
考点:酸的化学性质
专题:常见的酸 酸的通性
分析:碳酸钙能与盐酸反应生成二氧化碳气体,要探究是稀盐酸中的哪种粒子(H2O、H+、Cl-)能使碳酸钙溶解并产生无色气体,需排除一些离子的干扰,设计实验时要注意控制变量.
解答:解:(1)向①中加水,碳酸钙不溶解也无气体产生,说明通过实验①H2O不能使CaCO3溶解并产生无色气体,所以本题答案为:H2O不能使CaCO3溶解并产生无色气体;
(2)要证明是否是氢离子使碳酸钙溶解并产生气体,需加入含氢离子的物质,如硝酸,要证明是否是氯离子使碳酸钙溶解并产生气体,需加入含氯离子的物质,如氯化钠溶液,所以本题答案为:硝酸,氯化钠溶液;
(4)根据实验现象,可知是氢离子使碳酸钙溶解并产生气体,所以本题答案为:H+使CaCO3溶解并产生无色气体.
(2)要证明是否是氢离子使碳酸钙溶解并产生气体,需加入含氢离子的物质,如硝酸,要证明是否是氯离子使碳酸钙溶解并产生气体,需加入含氯离子的物质,如氯化钠溶液,所以本题答案为:硝酸,氯化钠溶液;
(4)根据实验现象,可知是氢离子使碳酸钙溶解并产生气体,所以本题答案为:H+使CaCO3溶解并产生无色气体.
点评:本题考查了碳酸钙与酸反应的实质,完成此题,要注意设计实验时变量的控制以及归纳法的应用.

练习册系列答案
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
下列实验操作后,溶液温度升高的是( )
①生石灰放入水中 ②NaOH固体溶于水中 ③浓硫酸倒入水中
④浓盐酸滴入浓烧碱中 ⑤NaCl晶体溶解于水中 ⑥NH4NO3晶体溶解于水中.
①生石灰放入水中 ②NaOH固体溶于水中 ③浓硫酸倒入水中
④浓盐酸滴入浓烧碱中 ⑤NaCl晶体溶解于水中 ⑥NH4NO3晶体溶解于水中.
| A、只有①② |
| B、有①②③④ |
| C、只有①②③ |
| D、有①②③④⑤⑥ |
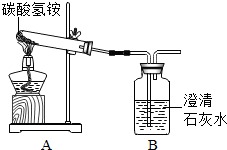 炎炎夏日,查理看到花园植物叶色发黄,于是给植物施用了碳酸氢铵肥料.他将肥料埋入靠近植物根部的土壤时,不小心将部分肥料洒落在干燥地面.可是,很快他发现洒落在地面的肥料消失了.针对洒落地面肥料消失的原因查理开展如下探究活动,请你参与并完成下列问题.【分析猜想】之一:被花园植物吸收了; 之二:被土壤溶液溶解了;
炎炎夏日,查理看到花园植物叶色发黄,于是给植物施用了碳酸氢铵肥料.他将肥料埋入靠近植物根部的土壤时,不小心将部分肥料洒落在干燥地面.可是,很快他发现洒落在地面的肥料消失了.针对洒落地面肥料消失的原因查理开展如下探究活动,请你参与并完成下列问题.【分析猜想】之一:被花园植物吸收了; 之二:被土壤溶液溶解了;
 我市正在逐步将管道煤气由石油液化气(主要成分是丁烷)改为天然气,小明家要进行灶具和燃气泄漏报警器的调整.请填空:
我市正在逐步将管道煤气由石油液化气(主要成分是丁烷)改为天然气,小明家要进行灶具和燃气泄漏报警器的调整.请填空: