题目内容
【题目】为了测定某碳酸氢钠纯度(含有少量氯化钠),某学生设计了图13装置:称取1.5g此样品于图13的试管中,滴加稀盐酸至不再产生气泡为止,观察到量气管装有油层的液面从400.0ml降到70.1ml。
【标况下![]() (CO2)≈2.0g/L 反应的化学方程式为:NaHCO3+HCl NaCl+H2O+CO2↑】
(CO2)≈2.0g/L 反应的化学方程式为:NaHCO3+HCl NaCl+H2O+CO2↑】
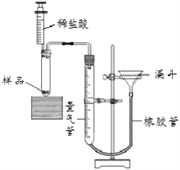
(1)反应结束时,收集到CO2质量。
(2)求该样品中NaHCO3的质量分数。
【答案】(1)0.66;(2)84%
【解析】(1)反应结束时,收集到CO2的体积为400.0mL70.0mL=330.0mL=0.33L,质量为:0.33L×2.0g/L=0.66g; (2)设碳酸氢钠的质量为![]() ,
,
NaHCO3+HCl═NaCl+H2O+CO2↑
84 44
x 0.66g
![]() ,
, ![]() =1.26g
=1.26g
该样品中NaHCO3的质量分数为![]() 。
。
答:该样品中NaHCO3的质量分数为84.0%。

【题目】臭氧(O3)是对于环境有重要影响的物质,兴趣小组对其进行如下探究。
【查阅资料】①O3微溶于水:
②O3常用于消毒等,但浓度超标时对人体有毒副作用;
③品红溶液为红色,遇强氧化剂(如O3)会变味无色。
探究一·臭氧的制备
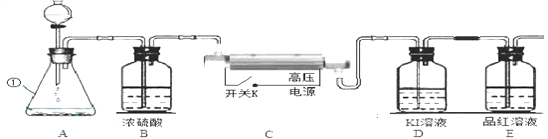
(1)写出仪器①名称___________。
(2)图中A装置制取氧气的化学方程式是______________。
(3)将A中制得的氧气一次通过图中B→E装置。
①B中浓硫酸的作用是____________________。
②实验开始,先通过一段时间氧气,合上C装置电源开关,在电火花作用下O2会转化为O3,该反应是____(填“物理”或“化学”)变化。
探究二·臭氧含量的测定
D中反应原理为:2KI+O3+H2O 2KOH+I2+O2,当E中出现现象时,可知D中反应完全。从安全、环保角度看,上述装置不足之处是____________。
(6)若D中生成碘12.7mg,则理论上应吸收O3_______mg(O3、I2的相对分子质量分别为48.254)。
探究三·影响臭氧分解的因素
O3在水中易分解,一定条件下,某浓度的O3在浓度减少一半所需的时间(t)如下表所示。
温度 分钟 pH | 3.0 | 4.0 | 5.0 | 6.0 |
20 | 301 | 231 | 169 | 58 |
30 | 158 | 108 | 48 | 15 |
40 | 31 | 26 | 15 | 7 |
(7)①分析表中数据,臭氧的分解速率与___________、___________有关。
②据表推测O3在下列条件下分解速率从小到大的顺序为___________(填序号)。
a.20℃、pH=3.0 b.30℃、pH=4.0 c.50℃、pH=6.0
③臭氧在水中分解是臭氧与水反应生成氧气和过氧化氢,反应的化学方程式为__________。
【题目】水善利万物
(1)水的组成:
下图是水电解实验,由此获得的信息是:
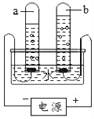
①a、b两极气体体积比为___________;
②该反应的化学方程式是____________。
(2)水的净化:
①生活中常通过____________方法降低水的硬度;
②经家用电解离子水器净化可得到酸、碱性不同的水,且各有其用途:
水的应用 | 浸泡蔬菜 | 日常饮用 | 烹饪 | 洗涤器皿 |
pH | 10.0 | 9.5 | 9.0 | 5.5 |
取上表用于____________的水样品中,滴入石蕊试液变红色。
(3)水的用途:
水是常见溶剂,下图为甲、乙、丙三种物质的溶解度曲线;
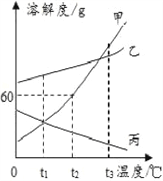
t1℃时,甲、乙、丙三种物质的溶解度大小关系是__________;
②t2℃时,甲的饱和溶液中溶质和溶剂的质量比为____________。