题目内容
(2011?塘沽区二模)水是生命之源,人类的日常生活与工农业生产都离不开水.
(1)天然水中含有许多杂质,向其中加入明矾,经溶解、静置、过滤,除去不溶性杂质.然后加入活性炭,利用其
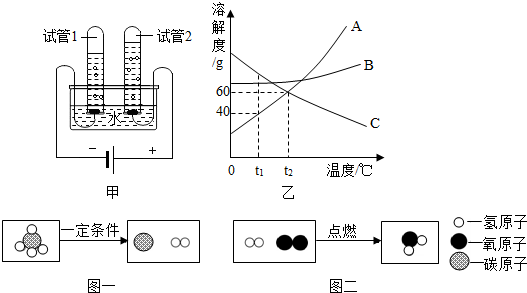
(2)用图甲所示.通电一段时间后,试管1中所收集的气体为
(3)图乙是A、B、C三种物质的溶解度曲线.请回答:
①t1℃时A、B、C三种物质的溶解度由大到小的顺序是
②当A中混有少量B时,可用
③在t1℃时,将25gA物质加入到盛有50g水的烧杯中,充分搅拌,再升温至t2℃(不考虑溶剂的挥发),在升温过程中,A溶液中溶质的质量分数的变化情况是
④氢气燃烧产物是水,被认为是最清洁的燃料,其制备及燃烧过程中会发生如下化学反应,反应的微观过程可用图一、图二表示:则参加反应的甲烷与生成水的质量之比为

(1)天然水中含有许多杂质,向其中加入明矾,经溶解、静置、过滤,除去不溶性杂质.然后加入活性炭,利用其
吸附
吸附
性除去异味,再杀菌消毒,得到生活用水,生活中常通过煮沸
煮沸
的方法降低水的硬度.(2)用图甲所示.通电一段时间后,试管1中所收集的气体为
氢气
氢气
,该实验说明水是由氢、氧两种元素组成的
水是由氢、氧两种元素组成的
(3)图乙是A、B、C三种物质的溶解度曲线.请回答:
①t1℃时A、B、C三种物质的溶解度由大到小的顺序是
CBA
CBA
②当A中混有少量B时,可用
降温结晶
降温结晶
方法提取纯A③在t1℃时,将25gA物质加入到盛有50g水的烧杯中,充分搅拌,再升温至t2℃(不考虑溶剂的挥发),在升温过程中,A溶液中溶质的质量分数的变化情况是
先逐渐增大,后保持不变
先逐渐增大,后保持不变
④氢气燃烧产物是水,被认为是最清洁的燃料,其制备及燃烧过程中会发生如下化学反应,反应的微观过程可用图一、图二表示:则参加反应的甲烷与生成水的质量之比为
4:9
4:9
.分析:(1)根据活性炭的吸附性、硬水软化的方法分析回答;
(2)根据电解水实验的现象和结论分析回答;
(3)①根据溶解度曲线的意义,比较某一温度时溶解度的大小;
②根据物质的溶解度随温度变化的情况,判断分离混合物的方法;
③根据溶解度进行有关的计算与分析.
④观察图示,找出甲烷与生成的水的微粒数目关系,再计算出质量比.
(2)根据电解水实验的现象和结论分析回答;
(3)①根据溶解度曲线的意义,比较某一温度时溶解度的大小;
②根据物质的溶解度随温度变化的情况,判断分离混合物的方法;
③根据溶解度进行有关的计算与分析.
④观察图示,找出甲烷与生成的水的微粒数目关系,再计算出质量比.
解答:解:(1)由于活性炭有吸附性,可除去天然水中的异味,生活中常通过煮沸的方法降低水的硬度.
(2)由电解水的装置可知,试管1中所收集的气体较多为氢气.电解水生成了氢气和氧气,说明了水是由水是由氢、氧两种元素组成的.
(3)①由A、B、C三种物质的溶解度曲线可知,在t1℃时A、B、C三种物质的溶解度由大到小的顺序是:C>B>A.
②由A、B的溶解度曲线可知,A的溶解度受温度的影响较大,B的溶解度受温度的影响不大,当A中混有少量B时,可用降温结晶方法提取纯A.
③由A的溶解度曲线可知,在t1℃时A的溶解是40g,由溶解度的含义可知,在t1℃时,将25gA物质加入到盛有50g水的烧杯中,充分搅拌,得到是饱和溶液,有未溶解的物质A,由于A的溶解度随温度的升高而增大.所以,再升温至t2℃(不考虑溶剂的挥发),在升温过程中,A溶液中溶质的质量分数的变化情况是先逐渐增大,后保持不变.
④由反应的微观过程图一、图二可知,参加反应的甲烷与生成的水的微粒的个数关系式是1:2.所以,参加反应的甲烷与生成水的质量之比为:(12+1×4):【2×(1×2+16】=4:9.
故答为:(1)吸附;煮沸.(2)氢气;由水是由氢、氧两种元素组成的.(3)①C>B>A;②降温结晶③先逐渐增大,后保持不变④4:9.
(2)由电解水的装置可知,试管1中所收集的气体较多为氢气.电解水生成了氢气和氧气,说明了水是由水是由氢、氧两种元素组成的.
(3)①由A、B、C三种物质的溶解度曲线可知,在t1℃时A、B、C三种物质的溶解度由大到小的顺序是:C>B>A.
②由A、B的溶解度曲线可知,A的溶解度受温度的影响较大,B的溶解度受温度的影响不大,当A中混有少量B时,可用降温结晶方法提取纯A.
③由A的溶解度曲线可知,在t1℃时A的溶解是40g,由溶解度的含义可知,在t1℃时,将25gA物质加入到盛有50g水的烧杯中,充分搅拌,得到是饱和溶液,有未溶解的物质A,由于A的溶解度随温度的升高而增大.所以,再升温至t2℃(不考虑溶剂的挥发),在升温过程中,A溶液中溶质的质量分数的变化情况是先逐渐增大,后保持不变.
④由反应的微观过程图一、图二可知,参加反应的甲烷与生成的水的微粒的个数关系式是1:2.所以,参加反应的甲烷与生成水的质量之比为:(12+1×4):【2×(1×2+16】=4:9.
故答为:(1)吸附;煮沸.(2)氢气;由水是由氢、氧两种元素组成的.(3)①C>B>A;②降温结晶③先逐渐增大,后保持不变④4:9.
点评:本题主要考查了水的净化、溶解度曲线的意义、反应的微观示意图的意义,难度变大,属于基础的知识,应加强基础知识的学习.

练习册系列答案
相关题目
