题目内容
【题目】(1)许多物质的命名与元素的化合价高低有关,如锰酸钾、高锰酸钾,其中锰元素的化合价分别为+6、+7.氯元素常见的化合价有+7、+5、+1、﹣1 等,由此推测钠元素、氧元素和+7价氯元素三种元素组成的化合物的名称为_________________,化学式为__________________________________。
(2)某种由 FeO 和 Fe2O3 组成的混合物中,两种组分的个数之比为 3:2,则 670g 混合物中 Fe 元素的质量是__________________________________g。
(3)测知Fe2O3和另一种氧化物的混合物中氧的含量为50%,则另一种氧化物可能是_________。
A SO2 B Na2O C CO2 D MgO
【答案】高氯酸钠 NaClO4 490 C
【解析】
(1)由题干可知,+7 价氯元素化合价最高,由钠元素、氧元素和+7 价氯元素三种元素组成的化合物名称中必有“高”,因为氧元素化合价一般为-2价,钠元素化合价一般为+1价,根据“某酸某”的命名原则可得,名称为:高氯酸钠,故填写:高氯酸钠;
根据化合物中正负化合价代数和为零原则可得,化学式为:NaClO4;
(2)设混合物中FeO的质量为x,Fe2O3的质量为y
①x+y=670g
②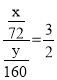
x=270g,y=400g
FeO中铁元素的质量为:270g×![]() ×100%=210g
×100%=210g
Fe2O3中铁元素的质量为:400g×![]() ×100%=280g
×100%=280g
670g混合物中 Fe 元素的质量是:210g+280g=490g
故填写:490;
(3)纯净的Fe2O3氧元素的质量分数为:![]() ×100%=30%,
×100%=30%,
题中给的数据是氧化铁中氧元素的质量分数与另一种氧化物中氧元素的质量分数的平均值,由于50%>30%,所以另一种氧化物中氧元素的质量分数必须要大于50%,
A、SO2中氧元素的质量分数=![]() ×100%=50%,故A不符合题意;
×100%=50%,故A不符合题意;
B、Na2O中氧元素的质量分数=![]() ×100%=25.8%,故B不符合题意;
×100%=25.8%,故B不符合题意;
C、CO2中氧元素的质量分数=![]() ×100%=72.7%,故C符合题意;
×100%=72.7%,故C符合题意;
D、MgO中氧元素的质量分数= ![]() ×100%=40%,故D不符合题意;故选:C。
×100%=40%,故D不符合题意;故选:C。