题目内容
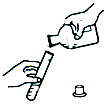
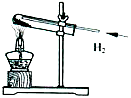
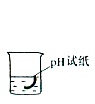
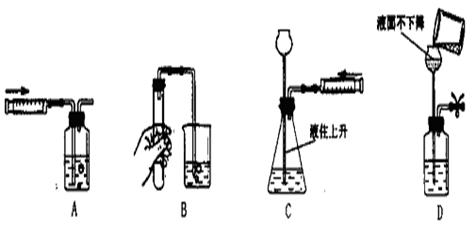
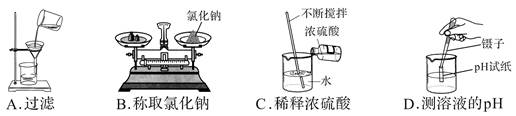
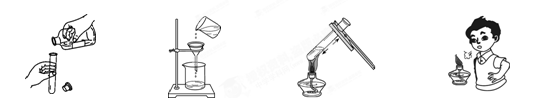
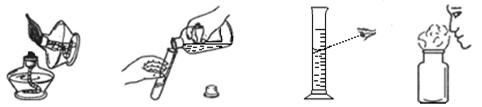
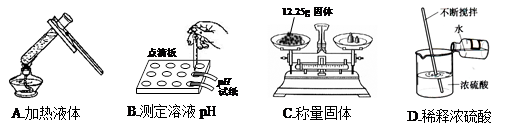
下图是配制50g质量分数为5% 的氯化钠溶液的操作过程示意图:

A B C D E
试回答:
(1)B操作中应称量氯化钠的质量是
(2)D操作应选用 mL 的量筒(从10 mL、50 mL中选择);量水时,量筒必须平放,视线要跟量筒凹液面的 处保持水平。
(3)E操作的作用是 。
(4)完成上述步骤后,将溶液转移至 里,并贴好标签。标签书写内容为:
(5)如果配制过程中出现以下情况可能造成对所配溶液的溶质质量分数的误差(填“偏高”、“偏低”、“无影响”):
①所用氯化钠药品不纯 ;
②量取水时俯视读数 ;
③配制完后将溶液转移至试剂瓶时洒出了一些 。

A B C D E
试回答:
(1)B操作中应称量氯化钠的质量是
(2)D操作应选用 mL 的量筒(从10 mL、50 mL中选择);量水时,量筒必须平放,视线要跟量筒凹液面的 处保持水平。
(3)E操作的作用是 。
(4)完成上述步骤后,将溶液转移至 里,并贴好标签。标签书写内容为:
(5)如果配制过程中出现以下情况可能造成对所配溶液的溶质质量分数的误差(填“偏高”、“偏低”、“无影响”):
①所用氯化钠药品不纯 ;
②量取水时俯视读数 ;
③配制完后将溶液转移至试剂瓶时洒出了一些 。
(1)2.5g (2)50;最低处 (3)加快溶解速度
(4)试剂瓶;氯化钠溶液5% (5)偏低 偏高 无影响
(4)试剂瓶;氯化钠溶液5% (5)偏低 偏高 无影响
试题分析:配制溶液的基本步骤是:计算、称量、量取、溶解、装瓶存放。
(1)根据公式,“溶质质量=溶液质量×溶质质量分数”计算,则需要氯化钠的质量为50g×5%=2.5g。
(2)量筒的选取原则是,量程要比所要量取的液体体积大且最接近的;而根据计算可知,配制该溶液所需水的量=50g-2.5g=47.5g,约合47.5ml(水的密度为1g/ml),故应选50ml的量筒;读取液体体积时,视线要跟量筒内凹液面的最低处保持水平。
(3)溶解时玻璃棒的作用是搅拌,能加速固体溶解。
(4)根据溶液的配制步骤可知,溶解后的溶液要装瓶存放,并贴好标签;标签书写内容应包括溶液的名称和溶质质量分数,故为5%的氯化钠溶液。
(5)根据溶质质量分数计算公式分析,如果配制的溶液溶质质量分数小于5%,有两种可能:称量的溶质少了(左码右物,或溶质中有杂质),量水量多了(仰视读数量水);如果配制的溶液溶质质量分数大于5%,则也有两种可能:称量的溶质多了(称量时指针偏左了),量水量少了(俯视读数量水);由于溶液具有均一性,故配制完后将溶液转移至试剂瓶时洒出了一些,不会影响配制的结果。
点评:熟记一定溶质质量分数的溶液的配制的基本步骤(计算、称量、量取、溶解、装瓶存放),以及操作的注意事项等,是解题的关键;此外,关于质量分数出现的误差要学会从溶质和溶剂两方面考虑。

练习册系列答案
相关题目