题目内容
【题目】某兴趣小组利用下列装置进行实验室制取和收集气体的实验,请回答:
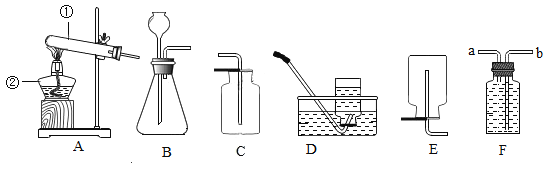
(1)指出仪器名称:①______;②_______。
(2)若用高锰酸钾制取氧气,应选用的发生装置是______(填字母)。你认为该装置中还缺少_________。写出该反应的文字表达式____________。
(3)若用过氧化氢制取氧气,还需要用到的物质是_______(填名称),其起到_______作用,写出用过氧化氢制氧气的文字表达式_________。
(4)用向上排空气法收集氧气,验满的方法是_________;若用F装置(装满水)收集氧气,则气体从___________端进入(填“a”或“b”)。
【答案】试管 酒精灯 A 棉花团 高锰酸钾![]() 锰酸钾+二氧化锰+氧气 二氧化锰 催化 过氧化氢
锰酸钾+二氧化锰+氧气 二氧化锰 催化 过氧化氢![]() 水+氧气 把带火星的木条放在集气瓶口,若木条复燃则集满 a
水+氧气 把带火星的木条放在集气瓶口,若木条复燃则集满 a
【解析】
(1)仪器①是试管,仪器②是酒精灯,故填:试管;酒精灯;
(2)若用高锰酸钾加热制取并收集氧气,需要加热,则应选用的装置是A,该装置中还缺少一团棉花,加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;故答案为:A;棉花团;高锰酸钾![]() 锰酸钾+二氧化锰+氧气;
锰酸钾+二氧化锰+氧气;
(3)过氧化氢分解制取氧气须加入二氧化锰作催化剂,过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的文字表达式是:过氧化氢![]() 水+氧气;故填:二氧化锰;催化;过氧化氢
水+氧气;故填:二氧化锰;催化;过氧化氢![]() 水+氧气;
水+氧气;
(4)因为氧气的密度比空气大,具有助燃性,用向上排空气法收集氧气,验满的方法是:把带火星的木条放在集气瓶口,若木条复燃则集满;因为氧气不易溶于水,密度比水小,若用F装置收集制得的氧气,则气体从a端进入;故填:把带火星的木条放在集气瓶口,若木条复燃则集满;a。

【题目】蚊虫叮咬时,会分泌蚁酸.化学小组同学对蚁酸产生了浓厚的兴趣,决定对其进行探究.
[提出问题]蚁酸的成分是什么?它有什么性质?
[查阅资料]I蚁酸的化学名称叫甲酸,化学式为HCOOH
II蚁酸隔绝空气并加热时会分解生成两种氧化物
Ⅲ浓硫酸具有吸水性
[实验探究](1)向盛有蚁酸溶液的试管中滴加紫色石蕊试液,观察到溶液颜色变成_____色,说明蚁酸显酸性.
(2)小芳同学根据蚁酸中含有______元素,推测出蚁酸在隔绝空气并加热分解时生成水.
(3)对它分解生成的另一种氧化物,小敏提出两种猜想:猜想Ⅰ是CO2; 猜想Ⅱ是____________;
他们按如图所示进行实验:先向装置中通入一会N2,再将蚁酸分解产生的气体通入其中.
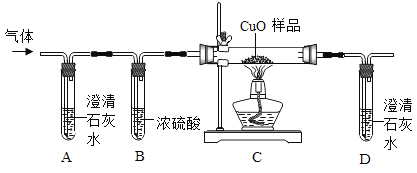
①先通N2的目的是_________________;
②若装置A中无明显变化,则猜想Ⅰ________(填“成立”或“不成立”);
③装置C发生反应的方程式为_______________________;
④装置D中的现象为_________________________;
[结论]甲酸受热能分解,反应的化学方程式是____________________;
[讨论交流]从环保角度看,该装置存在的明显缺陷是_________________.
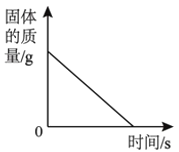
[拓展延伸]小组同学利用蚁酸分解产生的气体,测定C装置中10g氧化铜样品(杂质不参与反应)中氧化铜的质量分数,在不同时刻测定C中固体的质量(如表):
反应时间/min | 2 | 4 | 6 | 8 | 10 |
固体质量/g | 9.3 | 8.8 | 8.5 | 8.4 | 8.4 |
分析表中数据,完成以下问题:
①在称量质量过程中,必须把玻璃管两端封住,目的是_________________;
②样品中氧化铜的质量分数是________________?
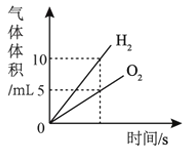
【题目】小美不小心将烧开的水洒在炽热的煤炉上(煤炉的燃料是焦炭),发现火焰突然升高,她感到好奇。在老师的指导下,小美得知水蒸气通过灼热的焦炭后得到某种混合气体,她决定对该混合气体的成分进行探究。
(提出问题)该混合气体有哪些成分?
(猜想与假设)Ⅰ.只有一氧化碳和水蒸气;Ⅱ.只有一氧化碳和氢气;
Ⅲ.含有一氧化碳、氢气和水蒸气。
(查阅资料)a.焦炭里的杂质不与水蒸气反应;
b.无水硫酸铜遇水由白色变为蓝色。
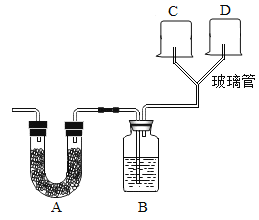
(实验方案)她设计了如图所示的实验装置,请你一并完成实验并填空。装置内盛放的物质依次为:A:无水硫酸铜;B:浓硫酸;C:内壁粘有澄清石灰水,D:内壁贴有吸附无水硫酸铜的石棉
(现象结论)
现象 | 分析 | 结论 |
①装置A中无水硫酸铜变蓝 | 混合气体中有__________ | 猜想____ 成立 |
②装置B中质量无变化 | ||
③装置C中澄清石灰水变浑浊 | 装置C中发生的化学反应方程式为_____ | |
④装置D中的现象为_____ | 混合气体燃烧有水生成 |
(反思评价)(1)装置B中浓硫酸的作用是_____________
(2)若将上述实验装置的方框部分用下图装置代替,也能得出相同的结论,则装置E中的现象为__________, F的作用为____________。

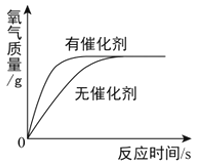
【题目】某化学兴趣小组的同学发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
[提出猜想]除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
[完成实验]按下表进行分析:测定分解温度(分解温度越低,催化效果越好)。
实验编号 | 实验药品 | 分解温度(°C) |
① | 氯酸钾 | 580 |
② | 氯酸钾、二氧化锰(质量比1:1) | 350 |
③ | 氯酸钾、氧化铜(质量比1:1) | 370 |
④ | 氯酸钾、氧化铁(质量比1:1) | 390 |
[分析数据、得出结论]
(1)实验室常用加热氯酸钾与二氧化锰的混合物的方法制取氧气,该反应的化学方程式为_____;
(2)实验所用的二氧化锰、氧化铜、氧化铁,催化效果最好的是_____;
(3)由实验_____与实验④对比,证明猜想合理。
(4)[反思]
①若要证明氧化铁是该反应的催化剂,还要验证它在化学反应前后的_____不变。
②上述对比实验中,氯酸钾与其它物质的质量比均为1:1,这样设计的目的是_____。
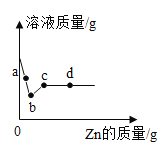
【题目】甲、乙、丙三位同学对氯化镁样品(仅含氯化钠杂质)进行如下检测:各取5.0g样品溶于一定量的水中得到25.0g溶液,再分别加入不同质量,溶质质量分数为10%的氢氧化钠溶液,反应得到沉淀的实验数据如下表
甲 | 乙 | 丙 | |
加入氢氧化钠溶液质量(g) | 35.0 | 40.0 | 45.0 |
反应得到沉淀的质量(g) | 2.5 | 2.9 | 2.9 |
试回答下列问题:
(1)上述实验中,_________同学所用的氢氧化钠溶液一定过量。
(2)求样品中氯化镁的质量分数_________(写出计算过程,结果精确到0.1%,下同)