题目内容
【题目】(1)买验室在稀释浓硫酸时,应将_____倒入_____中,并用玻璃棒不断搅动.
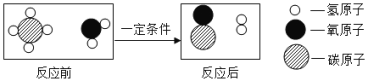
(2)在4Fe(OH)2+O2+2X=4Fe(OH)3↓化学反应中,反应物X的化学式是_____.
(3)如图所示,这是一瓶用排水法收集好的气体,据此,请你判断与这种气体相关的物理性质是:_____.
![]()
【答案】(1)浓硫酸;水;(2)H2O;(3)密度比空气大,不溶于水
【解析】
试题(1)稀释浓硫酸时,应该将浓硫酸倒入水中,并用玻璃棒不断搅拌,使产生的热量及时散失;(2)在4Fe(OH)2+O2+2X=4Fe(OH)3↓化学反应中,反应物中有4个铁原子、12个氢原子和12个氧原子,反应物中除了2X外有4个铁原子、10个氧原子和8个氢原子,即2X中含有4个氢原子和2个氧原子,一个X中含有2个氢原子和1个氧原子,故反应物X的化学式是 H2O;(3)通过气体的收集方法和集气瓶放置的方法可知,该气体的密度比空气大,不溶于水,另外还可知该气体为无色。

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目