题目内容
(2009?西宁)某兴趣小组探究酸碱中和反应,小明在盛有氢氧化钠溶液的试管中,滴加酚酞后,又滴加了稀盐酸,震荡后得到A溶液呈无色,他认为盐酸和氢氧化钠溶液恰好完全中和,
(1)写出该中和反应的化学方程式
(2)小红认为小明的结论不对.小红的观点是A溶液呈无色有两种可能,一种可能是
(3)请你设计一个实验,帮助他们确定A溶液中,酸、碱是否完全中和.填写实验报告.
(1)写出该中和反应的化学方程式
NaOH+HCl═NaCl+H2O
NaOH+HCl═NaCl+H2O
.(2)小红认为小明的结论不对.小红的观点是A溶液呈无色有两种可能,一种可能是
盐酸和氢氧化钠溶液恰好完全反应
盐酸和氢氧化钠溶液恰好完全反应
,另一种可能是盐酸过量
盐酸过量
.(3)请你设计一个实验,帮助他们确定A溶液中,酸、碱是否完全中和.填写实验报告.
| 实验步骤 | 实验现象及结论 |
取适量的反应后的溶液于试管中,然后向试管中加入锌粒, 取适量的反应后的溶液于试管中,然后向试管中加入锌粒, |
产生气泡,说明盐酸过量 产生气泡,说明盐酸过量 |
分析:(1)根据反应物和生成物即可写出反应方程式;
(2)氢氧化钠和稀盐酸反应生成硫氯化钠和水,而酚酞试液在酸性和中性溶液中均为无色,故无法判断是否恰好完全反应;
(3)若完全反应则溶液呈中性,若不是恰好完全反应,则呈酸性,因此可以从检验反应后的溶液中是否含酸着手设计实验即可
(2)氢氧化钠和稀盐酸反应生成硫氯化钠和水,而酚酞试液在酸性和中性溶液中均为无色,故无法判断是否恰好完全反应;
(3)若完全反应则溶液呈中性,若不是恰好完全反应,则呈酸性,因此可以从检验反应后的溶液中是否含酸着手设计实验即可
解答:解:(1)氢氧化钠和盐酸反应生成氯化钠和水,故可以写出该反应的化学方程式为:NaOH+HCl=NaCl+H2O;
(2)氢氧化钠和稀盐酸反应生成氯化钠和水,而酚酞试液在酸性和中性溶液中均为无色,所以该反应可能是恰好完全反应,也可能是盐酸过量;
(3)探究上述烧杯中的溶液是否恰好完全中和,可以检验反应后的溶液中是否含有盐酸来设计实验,选择的试剂可以是锌、紫色石蕊等能够和酸有明显反应现象的物质.
故答案为:(1)NaOH+HCl═NaCl+H2O;
(2)盐酸和氢氧化钠溶液恰好完全反应;盐酸过量;
(3)
(其它合理答案亦可).
(2)氢氧化钠和稀盐酸反应生成氯化钠和水,而酚酞试液在酸性和中性溶液中均为无色,所以该反应可能是恰好完全反应,也可能是盐酸过量;
(3)探究上述烧杯中的溶液是否恰好完全中和,可以检验反应后的溶液中是否含有盐酸来设计实验,选择的试剂可以是锌、紫色石蕊等能够和酸有明显反应现象的物质.
故答案为:(1)NaOH+HCl═NaCl+H2O;
(2)盐酸和氢氧化钠溶液恰好完全反应;盐酸过量;
(3)
| 实验步骤 | 实验现象及结论 |
| 取适量的反应后的溶液于试管中,然后向试管中加入锌粒, | 产生气泡,说明盐酸过量 |
点评:熟练掌握常见的酸和碱的化学性质,能够根据它们的性质选择合适的物质对它们进行验证是我们必须具备的能力.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
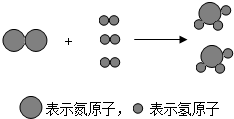 (2009?西宁)某化学反应的微观示意图如右图所示,下列说法正确的是( )
(2009?西宁)某化学反应的微观示意图如右图所示,下列说法正确的是( )