题目内容
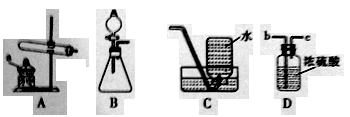
【题目】如图是实验室常用的两套装置。

①写出盛放药品 Y 的仪器名称________。
②若用甲装置制取氧气,则试剂 X 是________,反应的化学方程式________;用乙装置收集氧气, A 端应与________(填“B”或“C”)端相连。
③若 X 是稀盐酸、Y 是石灰石,用甲、乙两套装置可组成发生、净化、检验、收集 CO2 气体的系列装置。若要检验 CO2,乙中盛放的试剂及现象________
④若 X 是水,Y 是 CaC2 固体,可用于实验室制取乙炔(化学式:C2H2)气体,同时还生成一种碱,试写出反应的化学方程式_________。乙炔微溶于水,密度与空气接近,若用乙装置收集乙炔,则乙中应该装入_________。
【答案】锥形瓶 双氧水; ![]() ; B 澄清石灰水;澄清石灰水变浑浊 CaC2+2H2O→C2H2↑+Ca(OH)2; 水
; B 澄清石灰水;澄清石灰水变浑浊 CaC2+2H2O→C2H2↑+Ca(OH)2; 水
【解析】
①写出盛放药品 Y 的仪器名称是锥形瓶;
②若用甲装置制取氧气,反应物的状态是固体和液体,不需加热,应该是利用双氧水制取氧气,试剂X为双氧水,过氧化氢在二氧化锰的催化作用下分解生成氧气和水,化学方程式为:![]() ;氧气的密度大于空气,用乙装置收集氧气,A端口应与B端口相连;
;氧气的密度大于空气,用乙装置收集氧气,A端口应与B端口相连;
③二氧化碳能使澄清石灰水变浑浊,常用澄清石灰水检验二氧化碳。若 X 是稀盐酸、Y 是石灰石,用甲、乙两套装置可组成发生、净化、检验、收集 CO2 气体的系列装置。若要检验 CO2,乙中盛放的试剂是澄清石灰水,若澄清石灰水变浑浊,则该气体为二氧化碳;
④若 X 是水,Y 是 CaC2 固体,可用于实验室制取乙炔(化学式:C2H2)气体,同时还生成一种碱,根据质量守恒定律可知,该碱为氢氧化钙,反应的化学方程式为:CaC2+2H2O→C2H2↑+Ca(OH)2;乙炔微溶于水,可用排水法收集,密度与空气接近,不可用排空气法收集,若用乙装置收集乙炔,则乙中应该装入水。

 备战中考寒假系列答案
备战中考寒假系列答案【题目】据悉宣城高铁将于2020年开通,它将极大方便宣城人出行,也将为宣城发展带来机遇(如图所示)。钢铁和铝合金是建造高铁列车的主要金属材料。

(1)铝化学性质比铁活泼但比铁耐腐蚀,原因是___。在铁中熔入镍铬的目的是___。
(2)用一氧化碳和赤铁矿(主要成分为Fe2O3)炼铁的化学方程式是___。
(3)某生铁和钢的样品中,主要元素的质量分数如下表所示:
Fe | C | S | |
生铁 | 95.94% | 3.52% | 0.06% |
钢 | 98.97% | 0.45% | 0.03% |

结合数据及炼钢示意图(上图所示)生铁炼钢时通入过量氧气的目的是___,气体a的成分是___。