题目内容
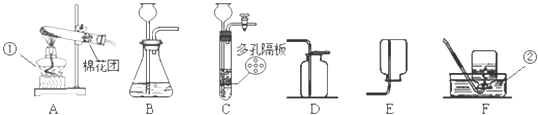
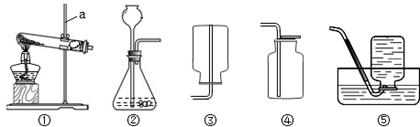
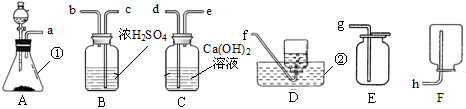
如图所示的是常用的实验装置。
(1)实验室用氯酸钾和二氧化锰固体制取氧气,为了制取和收集干燥的氧气应该选择的装置有(填序号)_____________。
(2)实验室可用__________装置(填装置序号)进行组装来制取二氧化碳。
(3)实验室可用①、⑥装置进行组装来制取______填化学式),请写出该反应的化学方程式_________。
(1)②③⑤ (2)①⑤ (3)H2 Zn+H2SO4=ZnSO4+H2↑
解析试题分析:制取装置包括加热和不需加热两种,如果用双氧水制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热。氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集。实验室制取CO2是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙、水和二氧化碳,因此不需要加热。二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法。实验室是用锌粒和稀硫酸在常温下反应制氢气,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集。
(1)如果用氯酸钾和二氧化锰制氧气就需要加热,要收集干燥的氧气,氧气可以用浓硫酸干燥,只能用向上排空气法收集。
(2)实验室制取CO2是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙、水和二氧化碳,因此不需要加热。二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法。
(3)实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集;锌粒和稀硫酸反应生成硫酸锌和氢气,反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑。
考点:考查常用气体的发生装置和收集装置与选取方法

 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案下表列出一氧化氮的部分性质(已知:空气在20℃时的密度是1.293 g / L)
| 物理性质 | 化学性质 | |||
| 熔点 | 沸点 | 密度(20℃) | 溶解性 | |
| -163.64℃ | -151.76℃ | 1.249 g / L | 不易溶于水 | 2NO+O2=2NO2 |
A.向上排气法 B.排水法 C.向下排气法 D.向下排气法或排水法
某气体只能用向上排空气法收集,则该气体具有的物理性质是( )
| A.能溶于水 | B.不易溶于水 |
| C.不会与空气中的成分发生反应 | D. |
常温下,某气体难溶于水,密度比空气小,则收集该气体可以采用的方法是 ( )
| A.向上排空气法 | B.排水法 |
| C.排水法或向上排空气法 | D.排水法或向下排空气法 |
某气体由氢气、一氧化碳、甲烷中的一种或几种组成,点燃该气体后,依次通过如图所示的装置,测得两装置的质量均增加,则下列对气体组成的推断正确的是( ) 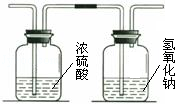
| A.可能只是甲烷,也可能只是一氧化碳 |
| B.可能只有氢气 |
| C.可能是甲烷和一氧化碳 |
| D.三种气体都一定存在 |