题目内容
14.监测某厂污水中有毒金属离子含量,需配制100克11%的氯化钠溶液.某学生按如图所示步骤顺序操作.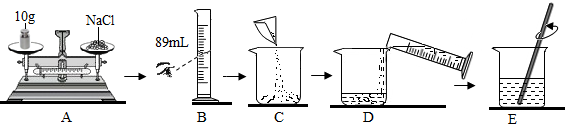
(1)以上步骤中有错误的是AB(用序号填充).操作错误应纠正为A处左码右物;B处视线应该与量筒内凹液面最低处保持水平.上述错误导致所配溶液溶质的质量分数小于11%.(填“大于”、“等于”、“小于”或“不确定”)
(2)E操作中玻璃棒的作用是搅拌,加快溶解.
(3)下列操作中不会影响所配溶液溶质质量分数的是CE(填字母).
A.称量操作中砝码和氯化钠放错盘
B.烧杯用水洗涤后未干燥就使用
C.量取水时平视量筒内凹液面最低处
D.量筒内的水没有全部倒入烧杯中
E.转移已配好的溶液时,有少量溶液溅出.
分析 (1)分析操作,判断存在错误的操作及所造成的后果,并加以改正;
(2)根据玻璃棒在操作中的作用解答;
(3)对操作带来的后果进行分析,判断对溶液质量分数不会造成影响的操作.
解答 解:(1)根据使用天平的原则,左物右码,图中左码右物,量筒的读数方法错误,视线应该与量筒内凹液面最低处保持水平;称量操作A中,砝码与药品放错位置,会使所称得的固体质量小于配制所需要溶质质量;量取溶剂水的B操作中,仰视读数,会使所量取的溶剂水的体积大于所读取的体积数,造成所取溶剂水的量大于配制所需要溶剂的量;通过这些操作所配制的溶液因溶质偏少、溶剂偏多而所得溶液的溶质质量分数小于所要配制溶液的质量分数11%;
(2)操作E为溶解操作,在此操作中玻璃棒起到搅拌以加快固体的溶解;
故答案为:搅拌,加快溶解;
(3)A、砝码与药品放错托盘会使所称取固体溶质质量偏小,造成所配制溶液的溶质质量分数偏小;
B、烧杯未干燥,杯壁有水,使得溶剂水偏多,溶液的溶质质量分数偏小;
C、量取时平视凹液面最低处,所量取的溶剂恰好为所需要水的量,对所得溶液的溶质质量分数没影响;
D、溶解时有水溅出而使溶剂量偏小,所得溶液的溶质质量分数偏大;
E、转移配制好的溶液时有少量液体溅出,由于溶液已配制完成,因此对所得溶液的溶质质量分数没有影响,只是所得溶液的量偏少;
故选CE.
答案:
(1)AB;A处左码右物;B处视线应该与量筒内凹液面最低处保持水平;小于;
(2)搅拌,加快溶解;
(3)CE.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、所需仪器、注意事项是正确解答本题的关键.造成所配制溶液的溶质质量分数偏大的原因,固体溶质量偏大与液体溶剂量偏小;反之亦反.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案
相关题目
4.化学改变世界的途径是使物质发生化学变化.下列属于化学变化的是( )
| A. | 冰块制成冰雕 | B. | 钨丝灯泡发光放热 | ||
| C. | 泥土烧成瓷器 | D. | 工业上从空气中分离出氧气 |
5.如图是元素周期表中的一种元素,下列有关该元素的信息正确的是( )


| A. | 原子序数是16 | B. | 它是金属元素 | ||
| C. | 核内质子数是32 | D. | 相对原子质量是16 |
9.下列关于四种粒子的结构示意图的说法中不正确的是( )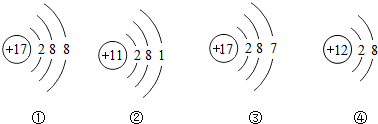

| A. | ①③属于同种元素 | |
| B. | ①④都属于离子,都是稳定结构 | |
| C. | ②③的化学性质相似 | |
| D. | ②④表示的元素在化合物中分别通常显+1和+2价 |
19.下列说法正确的是( )
| A. | 凡是含氧元素的化合物都是氧化物 | |
| B. | 二氧化锰可以作为所有化学反应的催化剂 | |
| C. | 不同种元素的最本质区别是质子数不同 | |
| D. | 空气中的氮气、氧气经混合,它们的化学性质都已改变 |
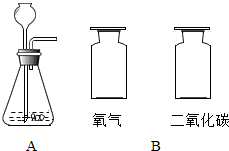 某校的兴趣小组的同学对目前市面上买的“发热贴”进行探究.通过实验探究发热贴是否真的只能与氧气反应发热,在缺氧的环境下(只有二氧化碳的环境)不能放热.
某校的兴趣小组的同学对目前市面上买的“发热贴”进行探究.通过实验探究发热贴是否真的只能与氧气反应发热,在缺氧的环境下(只有二氧化碳的环境)不能放热.