题目内容
【题目】化学是一门以实验为基础的科学,如图是实验室常用的制取气体的发生装置。
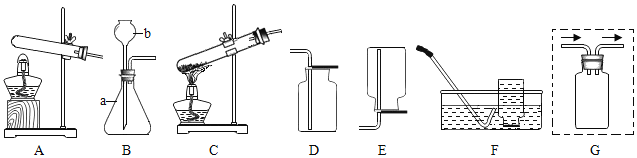
(1)写出仪器的名称。a:_____b:_____。
(2)若选用氯酸钾和二氧化锰为药品制取纯净的氧气,应选择的发生装置是_____(填写字母);反应的化学方程式:_____。若使用装置G排空气收集氧气,请在图中补充完整导管_____。
(3)选用5%的过氧化氢溶液和粉末状的二氧化锰混合制取氧气,应选择的发生装置是_____(填写字母)。为了控制反应的速率,可以将仪器b改为_____。
(4)汽车尾气中NO是一种大气污染物,它是一种无色气体,难溶于水,密度比空气略大,在空气中能与氧气迅速反应生成红棕色的NO2气体。实验室中制取NO采用的收集装置是_____(填写字母)。气体的性质是选择气体收集方法的主要依据,下列性质与收集方法的选择无关的是_____(填序号)。
①颜色 ②密度 ③溶解性 ④与空气成分是否反应
【答案】锥形瓶 长颈漏斗 A 2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑  B 分液漏斗(或注射器) F ①
B 分液漏斗(或注射器) F ①
【解析】
(1)通过分析题中所指仪器的名称和作用可知,a是锥形瓶,b是长颈漏斗;
(2)实验室用氯酸钾制取氧气的反应物是固体,反应条件是加热,所以应选择的发生装置是A,氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,化学方程式为:2KClO3![]() 2KCl+3O2↑,氧气密度比空气大,所以使用装置G排空气收集氧气的装置是:
2KCl+3O2↑,氧气密度比空气大,所以使用装置G排空气收集氧气的装置是: ;
;
(3)实验室用过氧化氢制取氧气的反应物是固体和液体,反应条件是常温,应选择的发生装置是B,分液漏斗可以控制液体的滴加速度,所以为了控制反应的速率,可以将仪器b改为分液漏斗(或注射器);
(4)一氧化氮难溶于水,密度比空气略大,在空气中能与氧气迅速反应生成红棕色的NO2气体,所以实验室中制取NO采用的收集装置是F,选择气体收集方法的主要依据是:密度、溶解性、与空气成分是否反应,故选①。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案【题目】化学教材中“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。请你一起参与他们的探究过程,并填写下列空白。
(问题)氧化铜![]()
![]() 能不能作过氧化氢
能不能作过氧化氢![]() 分解反应的催化剂呢?
分解反应的催化剂呢?
(猜想)______。
(实验验证)
实验 | 实验步骤 | 实验现象 | 实验结论 |
实验一 | 常温下,在试管中加入 | 有少量气泡产生,木条没有复燃 | 常温下 |
实验二 | 常温下,在装有 | 有较多气泡产生,木条复燃 | ______ |
(过论与反思)经过讨论,有的同学认为只有上述两个实验,不能证明CuO能作过氧化氢分解反应的催化剂,还要补充一个探充实验。
实验三:(实验目的)探究______。
(实验步骤)①准确称量![]() 少量
少量![]() 的质量;
的质量;
②重复实验二的步骤;待反应结束,将试管里的物质过滤,洗涤,干燥,称量;
③对比反应前后CuO的质量。
(讨论)如果______,则说明CuO能作过氧化氢分解反应的催化剂。但小茗同学认为,要证明猜想,上述三个实验还不足以说明,还需要再增加一个实验,以验证______。
(实验结论)CuO能作过氧化氢分解反应的催化剂,请写出CuO催化过氧化氢分解的文字表达式:______。
(拓展探究)同种催化剂,你还知道那些因素会影响过氧化氢分解反应的催化效果?假设:______。方案:______。