题目内容
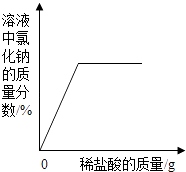
【题目】测定石灰石中的碳酸钙的含量,取出2.5克石灰石样品,逐渐加入稀盐酸,充分反应后测得剩余固体质量与加入稀盐酸的质量关系如图所示. 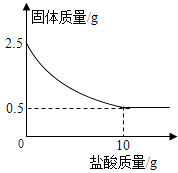
(已知杂质不参与反应,也不溶于水)
(1)石灰石样品中碳酸钙的质量是;
(2)石灰石样品中碳酸钙的质量分数是;
(3)计算反应产生的气体的质量(利用化学方程式计算).
【答案】
(1)2g
(2)80%
(3)解:设生成二氧化碳质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 44
2g x
![]() =
= ![]() ,
,
x=0.88g,
答:生成了0.88g二氧化碳.
【解析】解:(1)石灰石样品中杂质质量是0.5g,碳酸钙质量是:2.5g﹣0.5g=2g,
故填:2g.(2)石灰石样品中碳酸钙的质量分数为: ![]() ×100%=80%,
×100%=80%,
故填:80%.
【考点精析】本题主要考查了根据化学反应方程式的计算的相关知识点,需要掌握各物质间质量比=系数×相对分子质量之比才能正确解答此题.

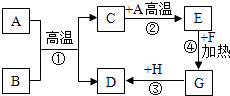
【题目】在高温下,铁与水蒸气能发生反应生成一种常见的铁的氧化物和一种气体.某兴趣小组请你参与研究:铁与水蒸气反应一段时间后剩余固体物质的成分、性质及再利用.
(1)【推断】①观察到D中黑色固体变红,则B中生成的气体是
②探究B装置中剩余固体成分是什么?
(2)【查阅资料】1.碎瓦片能防爆沸,碱石灰是氧化钙和氢氧化钠的混合物2.铁的氧化物中,只有Fe2O3是红棕色,其余均为黑色,只有Fe3O4能被磁铁吸引.
【初步探究】B装置中剩余固体为黑色,能全部被磁铁吸引
【猜想与假设】
猜想一:剩余固体是Fe3O4
猜想二:剩余固体是
(3)【实验探究】
实验操作 | 实验现象及结论 |
(4)【实验结论】铁与水蒸气反应的化学方程式为
(5)【成分再利用】若将B装置中剩余的黑色固体ag,经过一系列转化,全部变为红棕色固体Fe2O3(假设转化过程中铁元素无损耗),增加的质量为x,则x的取值范围为 .