题目内容
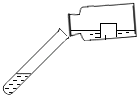
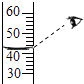
【题目】下图中的A﹣E是化学实验中常用的几种装置,请按要求回答有关问题. 
(1)利用上图中A、C装置的组合可以制取的一种气体是;写出实验室制取该气体的化学方程式: .
(2)若实验室制取二氧化碳气体,应选用图中装置的组合是;写出实验室制取二氧化碳气体的化学方程式: .
(3)写出实验室用锌与稀硫酸制取氢气的化学方程式: .
【答案】
(1)O2;2KClO3 ![]() 2KCl+3O2↑
2KCl+3O2↑
(2)B、D;CaCO3+2HCl═CaCl2+CO2↑+H2O
(3)Zn+H2SO4═ZnSO4+H2↑
【解析】解:(1)由题意知:图中A、C装置的组合可以制取的一种气体,符合反应需要加热,收集的气体不能与水反应或溶解,故为氧气;故制取氧气的化学方程式为:2KClO3 ![]() 2KCl+3O2↑;(2)实验室制取二氧化碳气体常温下进行,反应物为固体与液体反应,二氧化碳可溶于水,且密度比空气的大,故应选用上图中装置的组合是B、D;使用大理石与稀盐酸反应的化学方程式为:CaCO3+2HCl═CaCl2+CO2↑+H2O;(3)由题意可知,反应物为锌与稀硫酸,推测生成物为氢气和硫酸锌,故化学方程式为:Zn+H2SO4═ZnSO4+H2↑. 故答为:(1)O2;2KClO3
2KCl+3O2↑;(2)实验室制取二氧化碳气体常温下进行,反应物为固体与液体反应,二氧化碳可溶于水,且密度比空气的大,故应选用上图中装置的组合是B、D;使用大理石与稀盐酸反应的化学方程式为:CaCO3+2HCl═CaCl2+CO2↑+H2O;(3)由题意可知,反应物为锌与稀硫酸,推测生成物为氢气和硫酸锌,故化学方程式为:Zn+H2SO4═ZnSO4+H2↑. 故答为:(1)O2;2KClO3 ![]() 2KCl+3O2↑;(或2KMnO4
2KCl+3O2↑;(或2KMnO4 ![]() K2MnO4+MnO2+O2↑); (2)B、D; CaCO3+2HCl═CaCl2+CO2↑+H2O;(3)Zn+H2SO4═ZnSO4+H2↑
K2MnO4+MnO2+O2↑); (2)B、D; CaCO3+2HCl═CaCl2+CO2↑+H2O;(3)Zn+H2SO4═ZnSO4+H2↑
【考点精析】通过灵活运用氧气的制取装置和氢气的制取和检验,掌握发生装置:固固加热型、固液不加热型;氢气的实验室制法原理:Zn + H2SO4 = ZnSO4 +H2↑;Zn + 2HCl = ZnCl2 +H2↑不可用浓盐酸的原因 浓盐酸有强挥发性 ;不可用浓硫酸或硝酸的原因 浓硫酸和硝酸有强氧化性即可以解答此题.

 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案