题目内容
【题目】将等质量的锌粉和铁粉,分别放入相同质量分数的足量稀盐酸中,反应生成H2的质量与反应时间的关系如图所示,据图回答:
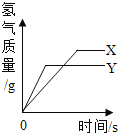
(1)金属X是______,判断的理由为______。
(2)从图中你还能获得的信息有______![]() 答一条即可
答一条即可![]() 。
。
【答案】铁 等质量的锌粉和铁粉分别放入相同质量分数的足量稀盐酸中,铁产生的氢气比锌多 锌比铁活泼(合理即可)
【解析】
分析图中可知,Y的反应时间要短,则Y比X活泼,X产生氢气要比Y的多。
(1)铁与盐酸反应的方程式为![]() ,参加反应铁的质量与生成氢气的质量比为56:2 ;锌与盐酸反应的方程式为
,参加反应铁的质量与生成氢气的质量比为56:2 ;锌与盐酸反应的方程式为![]() ,参加反应锌的质量与生成氢气的质量比为65:2。由质量比可知,等质量的锌粉和铁粉,分别放入相同质量分数的足量稀盐酸中,铁生成的氢气质量要大,锌生成的氢气质量要小。所以X是铁,Y是锌。
,参加反应锌的质量与生成氢气的质量比为65:2。由质量比可知,等质量的锌粉和铁粉,分别放入相同质量分数的足量稀盐酸中,铁生成的氢气质量要大,锌生成的氢气质量要小。所以X是铁,Y是锌。
(2)从图中可知,锌反应所需的时间要短,铁反应所需时间要长,说明锌比铁活泼。

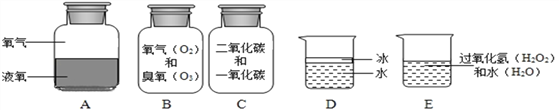
【题目】二氧化锰是不是过氧化氢溶液分解的唯一催化剂?对此小明设计了如下探究方案。
(提出问题)红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
(实验探究)
实验步骤 | 实验现象 | 实验结论及解释` |
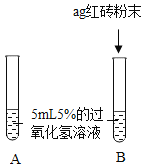
I.
| A中无明显现象,B中产生大量能使带火星木条复燃的气体。 | ①产生的气体是_________。 ②红砖粉末能改变过氧化氢分解速率。 |
Ⅱ.向B试管中重新加入5%的过氧化氢溶液;反应停止后过滤、洗涤、干燥、称量滤渣。 | B又产生大量能使带火星木条复燃的气体;滤渣质量等于ag。 | 红砖粉末的_______、_______在反应前后均没有发生变化,能作过氧化氢分解的催化剂。 |
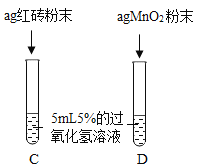
III.
| 两试管中均产生气泡且_______ 。 | 红砖粉末的催化效果没有二氧化锰粉末好。 |
请写出红砖粉末(成分以Fe2O3表示)催化过氧化氢溶液分解反应的化学方程式_______。
(反思)(1)小明在实验时发现试管内有许多水雾,由此推断过氧化氢分解是_______(填“放热”或“吸热”)反应。
(2)实验过程中发现将过氧化氢溶液加入红砖粉末的试管后,反应速率是逐渐加快,然后又逐渐变慢。从影响反应速率的因素来分析过氧化氢分解速率变化的原因________。