��Ŀ����
 A��B��C��D��E�dz��л�ѧ�г��������ֻ���������Ƕ�����һ����ͬ��Ԫ�أ���ͼ�Ǹ����ʼ��ת����ϵͼ������AΪʳ�ε���Ҫ�ɷ֣�B�к���Ԫ�أ�D��E����Һ������ɫ��������Һ��Ϊ��ɫ���ݺ͢�Ϊ�û���Ӧ��������Ϊ���ֽⷴӦ��
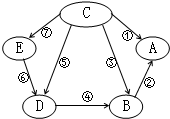
A��B��C��D��E�dz��л�ѧ�г��������ֻ���������Ƕ�����һ����ͬ��Ԫ�أ���ͼ�Ǹ����ʼ��ת����ϵͼ������AΪʳ�ε���Ҫ�ɷ֣�B�к���Ԫ�أ�D��E����Һ������ɫ��������Һ��Ϊ��ɫ���ݺ͢�Ϊ�û���Ӧ��������Ϊ���ֽⷴӦ����1��д���������ʵĻ�ѧʽ��A
NaCl
NaCl
��CHCl
HCl
����2��Eת��ΪDʱ������
�к�ɫ���ʲ�������Һ���dz��ɫ
�к�ɫ���ʲ�������Һ���dz��ɫ
����3�������
��Eת��ΪD�Ļ�ѧ����ʽ
CuCl2+Fe=Cu+FeCl2
CuCl2+Fe=Cu+FeCl2
����Cת��ΪE�Ļ�ѧ����ʽ
CuO+2HCl=CuCl2+H2O
CuO+2HCl=CuCl2+H2O
���÷�Ӧ�������ֽ�
���ֽ�
��Ӧ������������Ľ���ͻ�ƿ���AΪʳ�ε���Ҫ�ɷ֣���A���Ȼ��ƣ�B�к���Ԫ�أ���Ϊ�⼸�������ж�����ͬһ��Ԫ�أ���B���Ȼ�����D��E����Һ������ɫ���������Ȼ�ͭ���Ȼ��������Ȼ�����Һ����ΪE��ͨ���û���Ӧת������D����E�������Ȼ�ͭ��D�������Ȼ�������Cͨ���û���Ӧ�����Ȼ���������C����������ݴ˽��
����⣺AΪʳ�ε���Ҫ�ɷ֣���A���Ȼ��ƣ�B�к���Ԫ�أ���Ϊ�⼸�������ж�����ͬһ��Ԫ�أ���B���Ȼ�����D��E����Һ������ɫ���������Ȼ�ͭ���Ȼ��������Ȼ�����Һ����ΪE��ͨ���û���Ӧת������D����E�������Ȼ�ͭ��D�������Ȼ�������Cͨ���û���Ӧ�����Ȼ���������C���������ᣬ�����ͼ���ƶϺ�����
��1��A���Ȼ��ƣ�C�����ᣬ���NaCl��HCl��
��2���Ȼ�ͭ������Ӧ�����Ȼ�������ͭ����ͭ�Ǻ�ɫ�Ĺ��壬�Ȼ�������ˮ��Һ��dz��ɫ�ģ��ʻ�۲쵽�к�ɫ���ʲ�������Һ��Ϊdz��ɫ������к�ɫ���ʲ�������Һ���dz��ɫ��
��3����E���Ȼ�ͭ��D���Ȼ��������������Ȼ�ͭ��Ӧ����ͭ���Ȼ����������CuCl2+Fe=Cu+FeCl2��
��C�����ᣬE���Ȼ�ͭ��������������ͭ��Ӧ�����Ȼ�ͭ��ˮ���÷�Ӧ�Ǹ��ֽⷴӦ�����CuO+2HCl=CuCl2+H2O�����ֽ⣮
��1��A���Ȼ��ƣ�C�����ᣬ���NaCl��HCl��
��2���Ȼ�ͭ������Ӧ�����Ȼ�������ͭ����ͭ�Ǻ�ɫ�Ĺ��壬�Ȼ�������ˮ��Һ��dz��ɫ�ģ��ʻ�۲쵽�к�ɫ���ʲ�������Һ��Ϊdz��ɫ������к�ɫ���ʲ�������Һ���dz��ɫ��
��3����E���Ȼ�ͭ��D���Ȼ��������������Ȼ�ͭ��Ӧ����ͭ���Ȼ����������CuCl2+Fe=Cu+FeCl2��
��C�����ᣬE���Ȼ�ͭ��������������ͭ��Ӧ�����Ȼ�ͭ��ˮ���÷�Ӧ�Ǹ��ֽⷴӦ�����CuO+2HCl=CuCl2+H2O�����ֽ⣮
����������Ϊ��ͼʽ�����ƶ��⣬��ɴ��⣬�ؼ���������������������ͻ�ƿڣ�ֱ�ӵó��й����ʵĻ�ѧʽ��Ȼ�����ݿ�ͼ������ʵ������ƶϵó��������ʵĻ�ѧʽ��

��ϰ��ϵ�д�
 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�
�����Ŀ
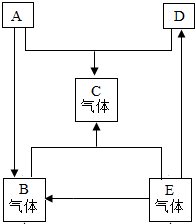 ��֪A��B��C��D��E�dz��л�ѧ�������������ʣ�����A��D�Ǻ�ɫ���壬AΪ��ɫ���嵥�ʣ�DΪ��ɫ��������������к�������ʹ����㷺�Ľ���Ԫ�أ�B��C��E����ɫ���壬��������һ�������µ�ת����ϵ����ͼ��ʾ��������Ӧ�������������ȥ����
��֪A��B��C��D��E�dz��л�ѧ�������������ʣ�����A��D�Ǻ�ɫ���壬AΪ��ɫ���嵥�ʣ�DΪ��ɫ��������������к�������ʹ����㷺�Ľ���Ԫ�أ�B��C��E����ɫ���壬��������һ�������µ�ת����ϵ����ͼ��ʾ��������Ӧ�������������ȥ���� 23����֪A��B��C��D��E�dz��л�ѧ�ﳣ�����������ʣ�������һ���������ܷ�����ͼ��ʾ��ת�������з�Ӧ���Ǹ��ֽⷴӦ��E���������ЧӦ����Ҫ���壮
23����֪A��B��C��D��E�dz��л�ѧ�ﳣ�����������ʣ�������һ���������ܷ�����ͼ��ʾ��ת�������з�Ӧ���Ǹ��ֽⷴӦ��E���������ЧӦ����Ҫ���壮 A��B��C��D��E�dz������ʣ�����B��E�ǿ������������壬C��������Ҫ�ɷ֣���ͼ��ʾ��ֱ�߱�ʾ����ܹ���Ӧ����ͷ��ʾת���ķ���
A��B��C��D��E�dz������ʣ�����B��E�ǿ������������壬C��������Ҫ�ɷ֣���ͼ��ʾ��ֱ�߱�ʾ����ܹ���Ӧ����ͷ��ʾת���ķ��� ��2013?���ݶ�ģ��A��B��C��D��E�dz��л�ѧ�г����IJ�ͬ�������ʣ����ʰ����ʡ�������ᡢ��η��ࣩ����֪A�ǵ��ʣ�C�Ǻ���ɫ���壻E��ˮ��Һ��ʹ��̪��Һ��Ϊ��ɫ���Σ�ͼ�С�-����ʾ��������������֮����Է�����Ӧ����������ʾ��ijһ���ʿ��Ƶ���һ���ʣ����ַ�Ӧ������P��Ӧ��������ȥ�����ش��������⣺
��2013?���ݶ�ģ��A��B��C��D��E�dz��л�ѧ�г����IJ�ͬ�������ʣ����ʰ����ʡ�������ᡢ��η��ࣩ����֪A�ǵ��ʣ�C�Ǻ���ɫ���壻E��ˮ��Һ��ʹ��̪��Һ��Ϊ��ɫ���Σ�ͼ�С�-����ʾ��������������֮����Է�����Ӧ����������ʾ��ijһ���ʿ��Ƶ���һ���ʣ����ַ�Ӧ������P��Ӧ��������ȥ�����ش��������⣺ A��B��C��D��E�dz��л�ѧ�г�����5�����ʣ����Ƕ�����һ����ͬ��Ԫ�أ���ͼ��ʾ������֮���ת����ϵ�����У�AΪʳ�ε���Ҫ�ɷ֣�B�к���Ԫ�أ�D��E����Һ������ɫ��
A��B��C��D��E�dz��л�ѧ�г�����5�����ʣ����Ƕ�����һ����ͬ��Ԫ�أ���ͼ��ʾ������֮���ת����ϵ�����У�AΪʳ�ε���Ҫ�ɷ֣�B�к���Ԫ�أ�D��E����Һ������ɫ��