题目内容
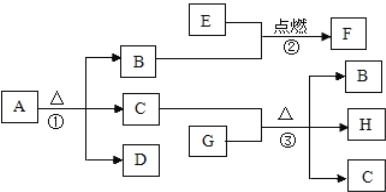
【题目】下图中A为一种混合气体,经分析只含有两种元素,根据图中的转化关系,回答下面的问题:

(1)写出下面各物质的化学式:
B_____________C_____________D____________
(2)写出下面的两个方程式:
C→D:_____________生成白色沉淀B:__________
【答案】CaCO3 CO Cu CO+CuO![]() CO2+Cu CO2+Ca(OH)2═CaCO3↓+H2O
CO2+Cu CO2+Ca(OH)2═CaCO3↓+H2O
【解析】
气体E通入紫色石蕊试液,溶液变红,可知此气体E为二氧化碳;气体C通过灼热的氧化铜,得到的红色物质D为铜,则气体C为一氧化碳;白色沉淀B与稀盐酸反应生成气体E二氧化碳,所以白色沉淀B为碳酸钙;把结论代入原题中验证,正好符合。
由分析可知(1)B为碳酸钙、C为一氧化碳、D为铜,化学式分别为:CaCO3、CO、Cu;
(2)①写出C→D,即“一氧化碳还原氧化铜制取铜”的化学方程式:CO+CuO![]() CO2+Cu;
CO2+Cu;
②生成白色沉淀B,即二氧化碳与澄清石灰水反应的化学方程式CO2+Ca(OH)2═CaCO3↓+H2O。

练习册系列答案
相关题目