��Ŀ����
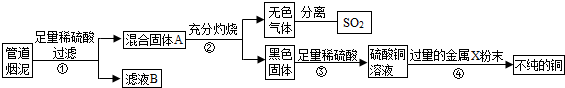
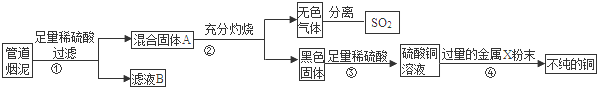
ij����ұ�����Ĺܵ������к���̿�ڼ�����ͭ��п�����ۺ�ʵ���С���ͬѧ����˴ӹܵ������л��ս���ͭ�����÷����еĶ��������Ʊ������ʵ�鷽����ʵ�������ͼ��ʾ��
��ش�
��1��������У����˲���ʹ���˲����������������� �����ȷ�������Ѿ������� ����
��2��������У�������Ľ���X��Zn�Ļ��˳����Zn��X������X���й㷺��;��X���� �����йط�Ӧ�Ļ�ѧ����ʽ�� ����
��3����ȥ����ͭ�е����ʽ���X����ѡ�õ��Լ�����Ʒ���� �������ţ���
a������ b��ϡ���� c������ˮ d���Ȼ�ͭ��Һ
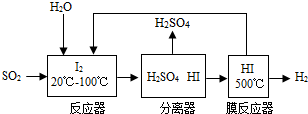
��4�����������SO2ͨ�����е�ѭ�����չ��̼�����H2SO4��������ȡH2�����������£�
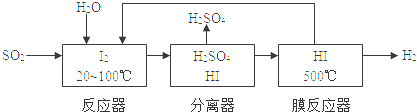
��д����Ӧ����Ĥ��Ӧ���еĻ�ѧ��Ӧ����ʽ�� ������ ����
��1��������ȡ������Һ�����Թ��ڣ����Թ��ڼ���п������������ݲ�����˵������������ǹ����ģ����û�����ݲ�����˵������û�й�������2��Fe��CuSO4+Fe��Cu+FeSO4����3��a��b��d��
��4��SO2+2H2O+I2��H2SO4+2HI��2HI H2+I2
H2+I2
��������
�����������1�����ݹ����в��������������÷����жϣ������������ʱ��Һ�лẬ�����ᣬ�ٸ��ݽ������ᷴӦ�����������з����жϡ��ڹ��˲����в����������������ã��Է�ֹҺ��ɽ�������п�Ļ������ǰ��ͭ�Ļ�����������ͭп�������ϡ���ᷴӦʱ��ͭ���ܲ��뷴Ӧ��̼Ҳ���ܷ�Ӧ����п��ϡ���ᷴӦ����������п�����Թ���ʱ��Һ������п������A��ͭ��̿�ڵĻ������������������ʱ����Һ�лẬ�����ᣬ����ȡ������Һ�����Թ��ڣ����Թ��ڼ���п������������ݲ�����˵������������ǹ����ģ����û�����ݲ�����˵������û�й�����
��2�����ݽ������˳���Ͻ���X���й㷺��;�����ý������������õ���صķ���ʽ�����������̼�������ɶ�����̼��ͭ������������ͭ������ͭ�������ת��������ͭ����Һ������ͭ�ӹ�����xͭ˵��x�Ļ�Ա�ͭǿ������������X��Zn�Ļ��˳����Zn��X������X���й㷺��;֪X�ǽ���������Ӧ����������ͭ�����û���Ӧ����Ӧ������������ͭд�ڵȺŵ���ߣ���������ͭ������������д�ڵȺŵ��ұߣ����Է���ʽΪ��CuSO4+Fe��Cu+FeSO4��
��3��������ͭ�����ʶ����߽��з��뼴�ɡ��������Ϲ������õIJ�����ͭ��ͭ��δ��Ӧ�����ۣ��ô�������������������ͭ�������ܷ��룬�����Ȼ�ͭ��Ӧ����ͭ���Ȼ�������ͭ���Ȼ�ͭ����Ӧ������Ҳ�ܷ��룬��ϡ����ʱͭ���ܷ�Ӧ�����ܣ�����ܷ������ߣ�����������ˮ���ܷ������ߣ�
��4�����ݻ�ѧ����ʽ����д�������DZ��⡣��Ӧ���еķ�Ӧ����ˮ���������⣬������������͵⻯�⣬���ݹ۲취��ƽ���ɣ����Է���ʽ�ǣ�SO2+2H2O+I2��H2SO4+2HI��Ĥ��Ӧ���еķ�Ӧ���ǵ⻯���������ǵ���������ù۲취��ƽ���ɣ����Է���ʽ�ǣ�2HI H2+I2��
H2+I2��
���㣺�������ʵ��ת�����Ʊ�

������Ʒ�в���Ԫ������������
| ��� | Cu | Zn | S |
| 1 | 10.3% | 5.0% | 1.2% |
| 2 | 11.5% | 4.9% | 1.8% |
| 3 | 12.4% | 10.3% | 0.9% |

��1��д������٢��к�ͭԪ�ص����ʷ�����Ӧ�Ļ�ѧ����ʽ��
��
��2��д���������д��������ķ������û�ѧ����ʽ��ʾ����
��3������������õIJ��������ǣ�
��4���ڲ�����У���ѡ���Լ�