题目内容
(7分)质量守恒定律是重要的三大定律之一,应用它可以帮助我们解决许多生产、科学实验和生活上的问题。现有氯酸钾和二氧化锰的混合物共26.5 g,加热使之反应,待反应至不再有气体生成后,将试管冷却、称量,得到剩余固体16.9g.求:
(1)制取氧气的质量共为___________ g。(2分);
(2)原混合物中氯酸钾多少克?(写出解题过程)(5分)
【答案】
(1)9.6g。(2分);(2)24.5 g
【解析】(1)加热氯酸钾和二氧化锰的混合物,氯酸钾受热分解生成氯化钾和氧气,二氧化锰在变化过程中为催化剂,反应前后质量和化学性质都不变;
利用质量守恒定律,由反应前后固体物质的质量差,可求得放出气体氧气的质量;
(2)根据反应的化学方程式,利用生成氧气的质量可计算完全反应后混合物中氯酸钾的质量.
(2)设原混合物中氯酸钾的质量为X:
2KClO3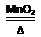 2 KCl + 3O2↑
2 KCl + 3O2↑
245 96
X 9.6g
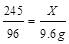
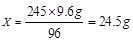
答:原混合物中氯酸钾的质量为24.5 g。

练习册系列答案
相关题目