题目内容
有一置于水中的用特殊材料制成的密闭容器,气体分子可以通过容器壁,液体固体则不能,其质量为1g,体积为0.04L,内装有32.7g 40%的硫酸溶液,如果向其中加入锌,要保持容器不下沉,锌的质量最多不超过
- A.6.3g
- B.6.5g
- C.7.5g
- D.13.0g
B
分析:利用锌与硫酸反应后的剩余质量加上1g容器质量,除以0.04L,所得的密度小于或等于1g/cm3,就不会下沉.
解答:设加入锌的质量为X,生成氢气质量为Y则:
Zn+H2SO4═ZnSO4+H2↑
65 2
X Y
根据: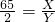 解得Y=
解得Y=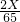 ;反应后剩余物质量为:32.7g+X-
;反应后剩余物质量为:32.7g+X-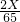 ,容器与容器内物质的总质量为:1g+32.7g+X-
,容器与容器内物质的总质量为:1g+32.7g+X-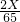 =33.7g+X-
=33.7g+X-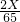 ,由于体积为0.04L=40mL,所以密度为:
,由于体积为0.04L=40mL,所以密度为: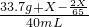 ,只要
,只要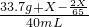 ≤1就不会下沉,解得X≤6.5g.
≤1就不会下沉,解得X≤6.5g.
故选B.
点评:解答本题的关键是要知道该容器要想不下沉,密度必须小于或等于水的密度.
分析:利用锌与硫酸反应后的剩余质量加上1g容器质量,除以0.04L,所得的密度小于或等于1g/cm3,就不会下沉.
解答:设加入锌的质量为X,生成氢气质量为Y则:
Zn+H2SO4═ZnSO4+H2↑
65 2
X Y
根据:
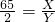 解得Y=
解得Y=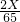 ;反应后剩余物质量为:32.7g+X-
;反应后剩余物质量为:32.7g+X-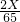 ,容器与容器内物质的总质量为:1g+32.7g+X-
,容器与容器内物质的总质量为:1g+32.7g+X-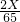 =33.7g+X-
=33.7g+X-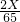 ,由于体积为0.04L=40mL,所以密度为:
,由于体积为0.04L=40mL,所以密度为: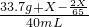 ,只要
,只要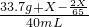 ≤1就不会下沉,解得X≤6.5g.
≤1就不会下沉,解得X≤6.5g.故选B.
点评:解答本题的关键是要知道该容器要想不下沉,密度必须小于或等于水的密度.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目