题目内容
【题目】下列化学方程式中符合题意且书写正确的是( )
A.正常雨水偏弱酸性原因:![]()
B.用稀硫酸除铁锈:![]()
C.用小苏打治疗胃酸过多症:![]()
D.工业上用熟石灰制取烧碱:![]()
【答案】C
【解析】
A、正常雨水偏弱酸性,是因为空气中的二氧化碳和水反应生成碳酸,反应的化学方程式为:CO2+H2O=H2CO3,该选项不正确;
B、铁锈主要成分是氧化铁,能和稀硫酸反应生成硫酸铁和水,反应的化学方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,该选项不正确;
C、用小苏打治疗胃酸过多症,是因为碳酸氢钠和稀盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:NaHCO3+HCl=NaCl+CO2↑+H2O,该选项正确;
D、氢氧化钙不能和硝酸钠反应,工业上用熟石灰和碳酸钠制取氢氧化钠,反应的化学方程式为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,该选项不正确。
故选:C。

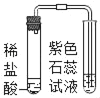
【题目】甲同学用如图所示装置制得CO2,并验证CO2能与水反应生成酸的性质。
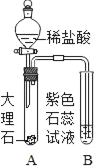
B试管发生的现象是_____,反应方程式是_____。
乙同学在实验时闻到制得的CO2有些刺激性气味,于是乙同学对气味的来源以及能使紫色石蕊溶液变红的酸性物质进行如下探究:
(查阅资料)大理石与稀盐酸反应产生热量;大理石无气味,稀盐酸有刺激性气味。
(提出猜想)刺激性气味来源于稀盐酸,并且混入与:
I.温度有关 II._____ III.温度及气流的速率有关
(进行实验)实验装置如下(三个实验中所用稀盐酸及紫色石蕊溶液的体积、溶质的质量分数均相同;夹持装置已略去)。
编号 | 实验装置及操作 | 实验现象与结论 |
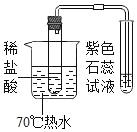
1 |
| 一段时间内无现象。 |
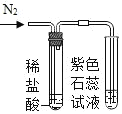
2 |
| 紫色石蕊试液变红,_____成立。 |
3 |
| _____,猜想II成立。综上猜想III成立。 |
(拓展与思考)
(1)需在装置A、B之间增加装置C.装置C的作用是_____,装置C中药品应具有的性质是_____。
(2)将实验1的稀盐酸改为浓盐酸,紫色石蕊试液变红,说明浓盐酸具有的物理性质是_____。
(3)有同学认为实验1可以省去不做也可以验证猜想。你的观点是_____(填“能”或“不能”)验证猜想。