题目内容
【题目】某同学为了研究生石灰CaO露置于空气中变质情况,设计如下实验:
取10克生石灰![]() 粉末A质量为12克
粉末A质量为12克![]() 气体B
气体B![]() 沉淀质量为2.5克
沉淀质量为2.5克
请通过分析计算:
(1)生成气体B的质量为______。
(2)粉末A中CaCO3的质量为______,这些CaCO3是由______克CaO转化而来的。
(3)粉末A的成分除CaO外还有______。(写化学式)
(4)粉末A中CaO的质量分数是多少?
【答案】(1)1.1g;(2)2.5g;1.4; (3)CaCO3、Ca(OH)2;(4)48.3%
【解析】
(1)设生成二氧化碳的质量为x,
气体B是二氧化碳,沉淀质量2.5g是二氧化碳和氢氧化钙反应生成碳酸钙的质量,则

x=1.1g
故填:1.1g。
(2)由CaCO3+2HCl═CaCl2+H2O+CO2↑,Ca(OH)2+CO2═CaCO3↓+H2O可知,粉末A中CaCO3的质量即为二氧化碳和氢氧化钙反应生成碳酸钙的质量,也是2.5g;
设这些CaCO3是由质量为y的CaO转化而来,
由CaO+H2O═Ca(OH)2,Ca(OH)2+CO2═CaCO3↓+H2O可知,CaO~CaCO3,则
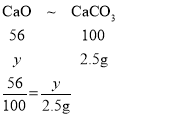
CaO~CaCO3,
y=1.4g,
故填:2.5g;1.4。
(3)1.4g氧化钙转化成2.5g碳酸钙后,固体质量增加:2.5g-1.4g=1.1g,因此氧化钙除部分转化成碳酸钙外,还有一部分转化成氢氧化钙,
设转化成氢氧化钙的氧化钙的质量为z,

z=2.8g,
粉末A中CaO的质量为:10g-1.4g-2.8g=5.8g,
粉末A中Ca(OH)2的质量为:12g-2.5g-5.8g=3.7g,
因此粉末A的成分除CaO外还有CaCO3、Ca(OH)2。
故填:CaCO3;Ca(OH)2。
(4)粉末A中CaO质量分数为:![]() ×100%=48.3%
×100%=48.3%
答:粉末A中CaO质量分数为48.3%。

【题目】如图是由传感器采集实验相关信息描绘出的曲线,其中物质x表示能与二氧化碳反应的某液体,纵坐标y表示烧杯中的某个量。下列相关分析正确的是( )
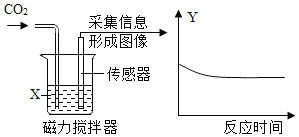
选项 | 物质X | 纵坐标y |
A | 水 | 溶液的质量 |
B | 水 | 溶液的PH |
C | 氢氧化钠溶液 | 溶质的质量 |
D | 氢氧化钙溶液 | 溶液中钙元素质量 |
A.AB.BC.CD.D