题目内容
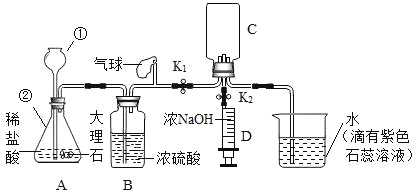
【题目】下图是甲、乙两位同学一起在实验室进行的氢氧化钠与盐酸中和反应的实验。
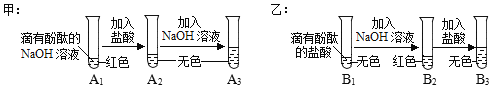
(说明:图中A1、A2、A3、B1、B2、B3均为溶液编号)
根据上图实验,请你与甲、乙同学一起完成下列探究:
探究环节 | 甲同学的探究 | 乙同学的探究 |
提出问题 | A3溶液为什么不变红? | B3溶液中溶质成分是什么?(酚酞不计) |
作出猜想 | 实验过程中,酚酞变质了。 | 猜想一:NaCl 猜想二:NaCl、HCl |
实验验证 | (1)取少量A3溶液于另一试管中,向其中滴加NaOH溶液,溶液变红,说明甲同学的猜想 (填“成立”或“不成立”)。 | 取少量B3溶液加入盛有少量铁粉的试管中,观察到有无色气泡产生,固体逐渐减少,溶液由无色变为 。据此,你认为乙同学的猜想 (填“一”或“二”)成立。 |
交流反思 | (1)甲、乙同学的实验中,反应均涉及到的化学方程式是 。 | |
【答案】【实验验证】:甲同学(1)不成立;(2)<; 乙同学:浅绿色; 二;【交流反思】(1)NaOH+HCl==NaCl+H2O; (2)盐酸;
【解析】试题分析:【实验验证】:甲同学(1)取少量A3溶液于另一试管中,向其中滴加NaOH溶液,溶液变红,说明甲同学的猜想不成立。说明盐酸过量或加入的氢氧化钠的质量太小;故(2)在常温下A2溶液测出的pH应<7;乙同学:根据B3能与金属铁反应产生气泡,故说明溶液中含有盐酸,反应后溶液中的颜色为浅绿色,说明猜想二成立;【交流反思】(1)甲、乙同学的实验中,反应均涉及到的化学方程式是NaOH+HCl==NaCl+H2O;(2)A3溶液未变红是因为盐酸过量的原因。

 中考解读考点精练系列答案
中考解读考点精练系列答案