题目内容
【题目】下列四个图像反映了对应实验过程中相关量的变化,其中不正确的是
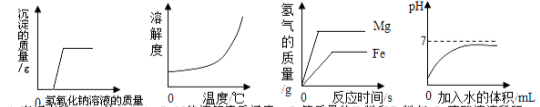




【答案】B
【解析】
试题分析:解答图像题,抓住“三点一走势”,即反应开始的一点,反应结束的一点,以及过量,A、在混有稀H2SO4的CuSO4溶液中滴加NaOH溶液,先发生反应:2NaOH+H2SO4==Na2SO4+2H2O,然后再发生反应:CuSO4+2NaOH==Cu(OH)2↓+Na2SO4,故沉淀质量刚开始是0,然后再不断增大,正确,B、气体的溶解度随温度的升高而降低,错误,C、等质量的Mg粉和Fe粉与足量同浓度的稀盐酸反应,由于Mg的活动性比Fe弱,故反应时间更短,且产生的氢气质量更大,正确,D、硫酸溶液稀释,酸性减弱,PH不断增大,无限制地接近7,正确,故选B

练习册系列答案
相关题目