题目内容
化学是一门以实验为基础的科学.研究物质的性质和变化是认识物质的重要手段.请根据反应事实写出下列反应的文字表达式,并回答有关问题.
(1)镁带在氧气中燃烧
(2)二氧化碳通入紫色石蕊试液
(3)二氧化碳通入澄清石灰水
(4)实验室用双氧水和二氧化锰制取氧气
上述反应中,属于化合反应的是
(1)镁带在氧气中燃烧
镁+氧气
氧化镁
| 点燃 |
镁+氧气
氧化镁
.镁粉常用来制作| 点燃 |
焰火、照明弹
焰火、照明弹
.(2)二氧化碳通入紫色石蕊试液
二氧化碳+水→碳酸
二氧化碳+水→碳酸
,观察到的现象是紫色石蕊试液变红
紫色石蕊试液变红
.(3)二氧化碳通入澄清石灰水
二氧化碳+氢氧化钙→碳酸钙+水
二氧化碳+氢氧化钙→碳酸钙+水
,观察到的现象是澄清石灰水变浑浊
澄清石灰水变浑浊
,若持续通入二氧化碳,你看到的现象是浑浊又变澄清
浑浊又变澄清
(4)实验室用双氧水和二氧化锰制取氧气
过氧化氢
水+氧气
| 二氧化锰 |
过氧化氢
水+氧气
,其中二氧化锰起| 二氧化锰 |
催化
催化
作用.用符号表示过氧化氢中氧元素的化合价H2
2
| -1 |
| O |
H2
2
.| -1 |
| O |
上述反应中,属于化合反应的是
(1)(2)
(1)(2)
,属于分解反应的是(4)
(4)
(填写序号).分析:根据反应物、生成物和反应条件,写出正确的文字表达式.根据反应物生成物的种类判断反应类型.
解答:解:(1)镁带在氧气中燃烧生成氧化镁,文字表达式为 镁+氧气
氧化镁.由于镁粉燃烧时发出白光,因此镁粉常用来制作 焰火、照明弹.
(2)二氧化碳通入紫色石蕊试液中,二氧化碳与水结合成碳酸,碳酸使紫色石蕊试液变红,文字表达式为 二氧化碳+水→碳酸.
(3)二氧化碳与澄清石灰水中的氢氧化钙反应生成不溶性的碳酸钙和水,因此石灰水变浑浊,文字表达式为 二氧化碳+氢氧化钙→碳酸钙+水,若持续通入二氧化碳,二氧化碳与碳酸钙和水反应生成易溶于水的碳酸氢钙,因此又由浑浊变澄清.
(4)双氧水在二氧化锰的催化作用下生成水和氧气,文字表达式为:过氧化氢
水+氧气,过氧化氢中氢元素+1价,氧元素为-1价,符号为 H2
2.
以上反应中(1)和(2)反应物是两种,生成物是一种,是化合反应,反应(4)中反应物是一种,生成物是两种,是分解反应.
故答案为:(1)镁+氧气
氧化镁. 焰火、照明弹.
(2)二氧化碳+水→碳酸,紫色石蕊试液变红.
(3)二氧化碳+氢氧化钙→碳酸钙+水,澄清石灰水变浑浊,浑浊又变澄清
(4)过氧化氢
水+氧气,催化 H2
2
| 点燃 |
(2)二氧化碳通入紫色石蕊试液中,二氧化碳与水结合成碳酸,碳酸使紫色石蕊试液变红,文字表达式为 二氧化碳+水→碳酸.
(3)二氧化碳与澄清石灰水中的氢氧化钙反应生成不溶性的碳酸钙和水,因此石灰水变浑浊,文字表达式为 二氧化碳+氢氧化钙→碳酸钙+水,若持续通入二氧化碳,二氧化碳与碳酸钙和水反应生成易溶于水的碳酸氢钙,因此又由浑浊变澄清.
(4)双氧水在二氧化锰的催化作用下生成水和氧气,文字表达式为:过氧化氢
| 二氧化锰 |
| -1 |
| O |
以上反应中(1)和(2)反应物是两种,生成物是一种,是化合反应,反应(4)中反应物是一种,生成物是两种,是分解反应.
故答案为:(1)镁+氧气
| 点燃 |
(2)二氧化碳+水→碳酸,紫色石蕊试液变红.
(3)二氧化碳+氢氧化钙→碳酸钙+水,澄清石灰水变浑浊,浑浊又变澄清
(4)过氧化氢
| 二氧化锰 |
| -1 |
| O |
点评:本题难度不大,主要考查了文字表达式的书写以及实验现象,从而加强学生对化学反应的理解

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
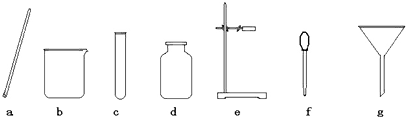
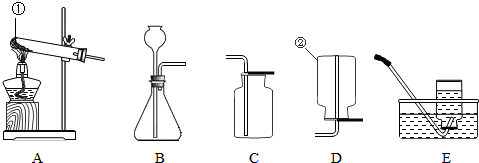
 20、化学是一门以实验为基础的科学,规范的实验操作是实验成功的前提,请回答:
20、化学是一门以实验为基础的科学,规范的实验操作是实验成功的前提,请回答: