题目内容
实验室常用下列装置来制取气体: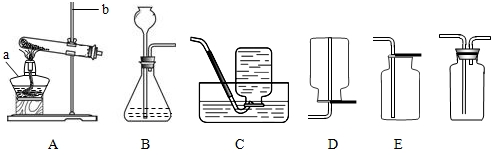
(1)写出图中有标号仪器的名称:a
(2)用双氧水和二氧化锰来制取氧气时,发生反应的化学方程式为
(3)用高锰酸钾制取氧气时,发生反应的化学方程式为.
(4)用E装置收集氧气的依据是
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,NH3极易溶于水.氨气在加热条件下能与氧化铜反应生成铜、水和空气中含量最多的气体.
①制取氨气反应的方程式:2NH4Cl+Ca(OH)2
| ||
②若用F装置来收集NH3,气体应从
③请写出氨气和氧化铜反应的化学方程式
(6)氢气是最清洁的燃料,它的密度比空气小,难溶于水,实验室常用锌粒与稀硫酸反应来制得.其化学方程式为
(7)小明用大理石与稀盐酸反应制取CO2,可选用的发生装置是
①下图是小明实验时的主要步骤,这些步骤的正确顺序是(填字母标号,下同)
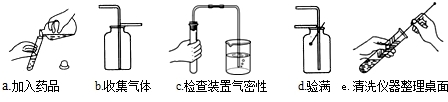
②加热固体碳酸氢钠或固体碳酸氢铵都能产生CO2,其方程式分别是:
NH4HCO3
| ||
2NaHCO3
| ||
乙同学利用加热碳酸氢钠的方法制取CO2,应该选用的发生装置是
他不选用碳酸氢铵制取CO2的理由是
③实验室里将用B装置制得的二氧化碳气体通入澄清石灰水中,始终未出现浑浊现象,可能的原因是
分析:(1)主要考查了对实验室常用仪器的认识;
(2)实验室用双氧水制取氧气时,要特别注意二氧化锰在化学方程式中的位置及二氧化锰的作用;
(3)根据实验室利用高锰酸钾分解制取氧气的原理可得化学方程式,注意条件是加热;
(4)密度比空气大的气体要采用向上排空气法收集气体;根据氧气验满方法作答即可;
(5)①根据质量守恒定律分析化学反应方程式可求得X的化学式
②NH3密度比空气小,要用向下排空气法收集;
③氨气与氧化铜生成单质铜,水和氮气;
(6)实验室用锌粒和稀硫酸制取氢气,氢气不溶于水且密度比空气小,要用排水法或向下排空气法收集;
(7)实验室制二氧化碳用的是大理石和稀硫酸,是属于“固液不加热型”,故选用B装置,二氧化碳密度比空气大,故用向上排空气法收集二氧化碳
①按照实验操作基本流程,实验操作基本步骤作答;
②碳酸氢钠为固体,反应需要加热,属于“固固加热型”;制取气体时生成物不能同时有两种气体,两种气体无法区别,收集到的是混合物.
③若盐酸太浓,盐酸要挥发,生成物中含有大量氯化氢气体,溶于水为盐酸,盐酸会和碳酸钙反应生成氯化钙和水.
(2)实验室用双氧水制取氧气时,要特别注意二氧化锰在化学方程式中的位置及二氧化锰的作用;
(3)根据实验室利用高锰酸钾分解制取氧气的原理可得化学方程式,注意条件是加热;
(4)密度比空气大的气体要采用向上排空气法收集气体;根据氧气验满方法作答即可;
(5)①根据质量守恒定律分析化学反应方程式可求得X的化学式
②NH3密度比空气小,要用向下排空气法收集;
③氨气与氧化铜生成单质铜,水和氮气;
(6)实验室用锌粒和稀硫酸制取氢气,氢气不溶于水且密度比空气小,要用排水法或向下排空气法收集;
(7)实验室制二氧化碳用的是大理石和稀硫酸,是属于“固液不加热型”,故选用B装置,二氧化碳密度比空气大,故用向上排空气法收集二氧化碳
①按照实验操作基本流程,实验操作基本步骤作答;
②碳酸氢钠为固体,反应需要加热,属于“固固加热型”;制取气体时生成物不能同时有两种气体,两种气体无法区别,收集到的是混合物.
③若盐酸太浓,盐酸要挥发,生成物中含有大量氯化氢气体,溶于水为盐酸,盐酸会和碳酸钙反应生成氯化钙和水.
解答:解:(1)通过分析实验室常用仪器的名称可知:a、酒精灯,b、长颈漏斗;
(2)实验室用双氧水制取氧气的化学方程式为:2H2O2
2H2O+O2↑;
因为二氧化锰在化学反应前后化学性质和质量不变可知二氧化锰是催化剂,故答案为:催化.
(3)用高锰酸钾制取氧气时要特别注意需要加热,化学方程式为:2KMnO4
K2MnO4+MnO2+O2↑.
(4)因为氧气的密度比空气大,所以可用E装置向上排空气法收集,故答案为:氧气的密度比空气大;
检验氧气是否集满方法:用带火星的木条伸到集气瓶口.
(5)①通过分析化学反应方程式可知X的化学式,故答案为:H2O;
②因为NH3密度比空气小,需用用向下排空气法,而从N导管口进入为向下排空气法,故答案为:N;
③氨气与氧化铜反应的化学方程式为:2NH3+3CuO
3Cu+3H2O+N2↑.
(6)实验室用锌粒和稀硫酸制取氢气的化学方程式为:Zn+H2SO4═ZnSO4+H2↑;
∵氢气不溶于水且密度比空气小,∴可用排水法和向下排空气法收集;
收集装置中C为排水法,D为向下排空气法,E从N端进入时为向下排空气法,故选CDF.
(7)反应物为固体时可用A装置:启普发生器,反应物为固体和液体时可用B装置;
实验室制二氧化碳用的是大理石和稀硫酸,大理石为固体,稀硫酸为液体,故选B.
二氧化碳密度比空气大,故用向上排空气法收集;收集装置中,E为向上排空气法,F从M端进入时为向上排空气法,
故答案为:EF.
①按照实验操作基本流程,实验操作基本顺序为:检验装置气密性、加入药品、收集气体、验满、清洗仪器、整理桌面,故选Cabde
氧气验满的正确方法为:用带火星小木条伸到集气瓶口,d图示中将带火星的小木条伸到了集气瓶中,故选D
②∵加热碳酸氢铵生成二氧化碳和氨气两种气体,收集到的气体为混合物,故不能用碳酸氢铵制取二氧化碳,故选A生成物中有两种气体
③制取二氧化碳应用大理石和稀盐酸,若盐酸太浓,盐酸要挥发产生氯化氢气体,生成物中会含有大量氯化氢气体,澄清石灰水不会变混浊,故答案为:盐酸太浓
(2)实验室用双氧水制取氧气的化学方程式为:2H2O2
| ||
因为二氧化锰在化学反应前后化学性质和质量不变可知二氧化锰是催化剂,故答案为:催化.
(3)用高锰酸钾制取氧气时要特别注意需要加热,化学方程式为:2KMnO4
| ||
(4)因为氧气的密度比空气大,所以可用E装置向上排空气法收集,故答案为:氧气的密度比空气大;
检验氧气是否集满方法:用带火星的木条伸到集气瓶口.
(5)①通过分析化学反应方程式可知X的化学式,故答案为:H2O;
②因为NH3密度比空气小,需用用向下排空气法,而从N导管口进入为向下排空气法,故答案为:N;
③氨气与氧化铜反应的化学方程式为:2NH3+3CuO
| ||
(6)实验室用锌粒和稀硫酸制取氢气的化学方程式为:Zn+H2SO4═ZnSO4+H2↑;
∵氢气不溶于水且密度比空气小,∴可用排水法和向下排空气法收集;
收集装置中C为排水法,D为向下排空气法,E从N端进入时为向下排空气法,故选CDF.
(7)反应物为固体时可用A装置:启普发生器,反应物为固体和液体时可用B装置;
实验室制二氧化碳用的是大理石和稀硫酸,大理石为固体,稀硫酸为液体,故选B.
二氧化碳密度比空气大,故用向上排空气法收集;收集装置中,E为向上排空气法,F从M端进入时为向上排空气法,
故答案为:EF.
①按照实验操作基本流程,实验操作基本顺序为:检验装置气密性、加入药品、收集气体、验满、清洗仪器、整理桌面,故选Cabde
氧气验满的正确方法为:用带火星小木条伸到集气瓶口,d图示中将带火星的小木条伸到了集气瓶中,故选D
②∵加热碳酸氢铵生成二氧化碳和氨气两种气体,收集到的气体为混合物,故不能用碳酸氢铵制取二氧化碳,故选A生成物中有两种气体
③制取二氧化碳应用大理石和稀盐酸,若盐酸太浓,盐酸要挥发产生氯化氢气体,生成物中会含有大量氯化氢气体,澄清石灰水不会变混浊,故答案为:盐酸太浓
点评:常见气体的发生和收集装置需同学们准确掌握,常见方程式的书写是同学们必须准确掌握的.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

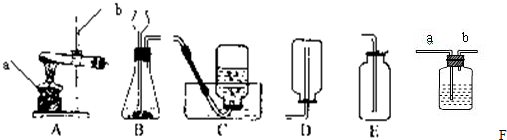

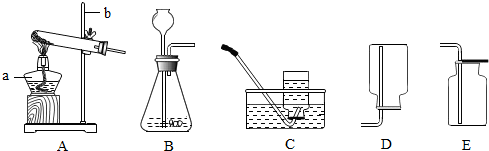
 实验室常用下列装置来制取氧气:
实验室常用下列装置来制取氧气: