题目内容
20g10%氢氧化钠溶液中,加入20g10%的硫酸,充分反应后,向混合物中滴加几滴无色酚酞试剂,溶液的颜色为
- A.变蓝色
- B.不变色
- C.变红色
- D.无法判断
C

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案
相关题目
为探究“酸碱中和反应”,进行了如下研究.
【实验原理】将稀HCl滴入盛有NaOH溶液的烧杯中,反应的化学方程式为______;
【提出问题】实验中未观察到明显现象,同学们对该反应是否发生提出了疑问:反应后溶液中溶质是什么?
【假设猜想】溶液中的溶质有氯化钠,还可能有:
猜想1:HCl
猜想2:NaOH
猜想3:HCl和NaOH
你认为上述猜想不合理的是______.
【实验方案】(1)某同学用一支洁净试管取少量烧杯中的溶液,滴加FeCl3溶液,无明显现象,说明烧杯中溶液里一定不含______;
(2)为了验证其余猜想,各小组进行如下三个方案的探究.
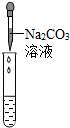
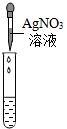
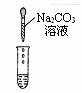
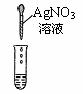
| 实验方案 | 甲 | 乙 | 丙 |
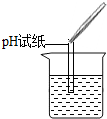
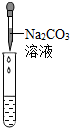
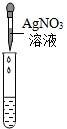
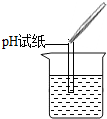
实验操作 |  | 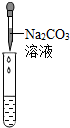 | 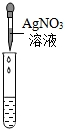 |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | ______ | 产生白色沉淀 |
| 实验结论 | 溶液中有HCl | 溶液中有HCl | 溶液中有HCl |
①实验操作中的错误是______;
②实验结论中也有一个是错误的,错误的原因是______;
通过对上述实验的正确操作,同学们得出了正确的结论.
你认为【假设猜想】中______是正确的.
(3)在20g10%的氢氧化钠溶液中加入25g稀盐酸恰好完全反应.
①计算氢氧化钠的物质的量为______;
②计算25g稀盐酸中溶质的质量分数______(计算结果精确到0.1%).(根据化学方程式列式计算)
为探究“酸碱中和反应”,进行了如下研究。
【实验原理】将稀HCl滴入盛有NaOH溶液的烧杯中,反应的化学方程式为 ;
【提出问题】实验中未观察到明显现象,同学们对该反应是否发生提出了疑问:反应后溶液中溶质是什么?
【假设猜想】溶液中的溶质有氯化钠,还可能有:
猜想1:HCl
猜想2:NaOH
猜想3:HCl和NaOH
你认为上述猜想不合理的是 。
【实验方案】(1)某同学用一支洁净试管取少量烧杯中的溶液,滴加FeCl3溶液,无明显现象,说明烧杯中溶液里一定不含 ;
(2)为了验证其余猜想,各小组进行如下三个方案的探究。
| 实验方案 | 甲 | 乙 | 丙 |
| 实验操作 |
|
|
|
| 实验现象 | 试纸变色,对比比色卡,pH<7 |
| 产生白色沉淀 |
| 实验结论 | 溶液中有HCl | 溶液中有HCl | 溶液中有HCl |
【推论与分析】上述实验方案中有两处明显错误:
 ①实验操作中的错误是 ;
①实验操作中的错误是 ;
②实验结论中有一个是错误的,错误的原因是 ;
通过对上述实验的正确操作,同学们得出了正确的结论。
你认为【假设猜想】中 是正确的。
(3)在20g10%的氢氧化钠溶液中加入25g稀盐酸恰好完全反应。
计算25g稀盐酸中溶质的质量分数 (计算结果精确到0.1%)。
为探究“酸碱中和反应”,进行了如下研究.
【实验原理】将稀HCl滴入盛有NaOH溶液的烧杯中,反应的化学方程式为______;
【提出问题】实验中未观察到明显现象,同学们对该反应是否发生提出了疑问:反应后溶液中溶质是什么?
【假设猜想】溶液中的溶质有氯化钠,还可能有:
猜想1:HCl
猜想2:NaOH
猜想3:HCl和NaOH
你认为上述猜想不合理的是______.
【实验方案】(1)某同学用一支洁净试管取少量烧杯中的溶液,滴加FeCl3溶液,无明显现象,说明烧杯中溶液里一定不含______;
(2)为了验证其余猜想,各小组进行如下三个方案的探究.
【推论与分析】上述实验方案中有两处明显错误:
①实验操作中的错误是______;
②实验结论中也有一个是错误的,错误的原因是______;
通过对上述实验的正确操作,同学们得出了正确的结论.
你认为【假设猜想】中______是正确的.
(3)在20g10%的氢氧化钠溶液中加入25g稀盐酸恰好完全反应.
①计算氢氧化钠的物质的量为______;
②计算25g稀盐酸中溶质的质量分数______(计算结果精确到0.1%).(根据化学方程式列式计算)
【实验原理】将稀HCl滴入盛有NaOH溶液的烧杯中,反应的化学方程式为______;
【提出问题】实验中未观察到明显现象,同学们对该反应是否发生提出了疑问:反应后溶液中溶质是什么?
【假设猜想】溶液中的溶质有氯化钠,还可能有:
猜想1:HCl
猜想2:NaOH
猜想3:HCl和NaOH
你认为上述猜想不合理的是______.
【实验方案】(1)某同学用一支洁净试管取少量烧杯中的溶液,滴加FeCl3溶液,无明显现象,说明烧杯中溶液里一定不含______;
(2)为了验证其余猜想,各小组进行如下三个方案的探究.
| 实验方案 | 甲 | 乙 | 丙 |
实验操作 |  | 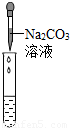 | 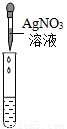 |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | ______ | 产生白色沉淀 |
| 实验结论 | 溶液中有HCl | 溶液中有HCl | 溶液中有HCl |
①实验操作中的错误是______;
②实验结论中也有一个是错误的,错误的原因是______;
通过对上述实验的正确操作,同学们得出了正确的结论.
你认为【假设猜想】中______是正确的.
(3)在20g10%的氢氧化钠溶液中加入25g稀盐酸恰好完全反应.
①计算氢氧化钠的物质的量为______;
②计算25g稀盐酸中溶质的质量分数______(计算结果精确到0.1%).(根据化学方程式列式计算)