题目内容
【题目】一定条件下,三种物质在密闭容器中发生反应,反应前后物质的质量比例如下图所示。以下说法正确的是

A. 反应中CaO为催化剂 B. 该反应是复分解反应
C. 反应后容器中固体总质量减少 D. 反应后容器中氧元素质量分数增大
【答案】C
【解析】质量增加的物质为生成物,质量减少的物质为反应物;由图可知,二氧化碳、氧化钙的质量增加,是生成物;碳酸钙的质量减少,是反应物。所以反应为碳酸钙生成氧化钙和二氧化碳,是分解反应。由质量守恒定律可知,反应前后物质的总质量不变,所以碳酸钙的质量等于氧化钙和二氧化碳的质量和,所以反应后容器中固体总质量减少;由质量守恒定律可知,反应前后元素的种类、质量不变。反应后容器中氧元素质量不变。选C

 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案【题目】下列图像与对应的表述一致的是

实验 | x轴表示的含义 | y轴表示的含义 | |
A | 将MnO2放入双氧水中 | 时间(s) | 溶液中水的质量(g) |
B | 足量红磷在装有空气的 密闭的集气瓶中燃烧 | 时间(s) | 瓶内气体的体积(mL) |
C | 向白色硫酸铜粉末中 逐滴滴加水 | 水的质量(g) | 溶液的质量(g) |
D | CO与CuO反应 | 通入CO的物质的量(mol) | CuO的物质的量(mol) |
A. A B. B C. C D. D
【题目】实验室常用的制取气体的发生装置如下:

(1)搭建B装置时,酒精灯应在固定仪器a之 (选填(“前” 或“后”)放置,实验结束时应
(2)在实验室制取二氧化碳的研究中,进行了如下实验:
试验编号药品 | 甲 | 乙 | 丙 | 丁 |
大理石 | mg,块状 | mg,块状 | mg,粉末状 | mg,粉末状 |
盐酸(过量) | wg,稀盐酸 | wg,浓盐酸 | wg,稀盐酸 | wg,浓盐酸 |
Ⅰ.上述实验中反应的化学方程式是 .
Ⅱ.若要研究盐酸浓度大小对反应的影响,可选择实验乙与 对照(选填实验编号)
Ⅲ.除盐酸的浓度外,上述实验研究的另一个影响反应快慢的因素是 .
(3)Ⅰ.研究发现酸浓度越大,产生气体的速度越快;浓盐酸有挥发性。与甲比较,对丁分析正确的是 (选填编号)
a.反应更为剧烈 b.最终反应装置中剩余物质的质量更小
c.产生二氧化碳的质量更大 d.粉末状大理石利用率更高
Ⅱ.下表中的两个实验,尽管在原料状态、发生装置等方面存在差异,却都能控制气体较平稳的产生.请从实验目的、原理、原料、装置、操作等方面思考后,具体阐述每个实验中气体较平稳产生的最主要的一个原因。
目的 | 原料 | 发生装置 | 气体较平稳产生的最主要的一个原因 |
制取二氧化碳 | 块状大理石 稀盐酸 | A | |
制取氧气 | 粉末状二氧化锰 3%的过氧化氢溶液 | C |
【题目】某白色固体A可能含有碳酸钠、氧化钙、氯化钠中的一种或几种,进行如下实验:
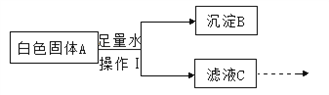
完成下列问题:
①操作I的名称是___________。根据上述实验流程分析,A中一定含有的物质是__________,C中一定含有的溶质是________。
②为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成下表。
实验操作 | 现象 | 结论 |
用一支洁净的试管取适量滤液C,___________。 | _________________ | A中有氯化钠 |