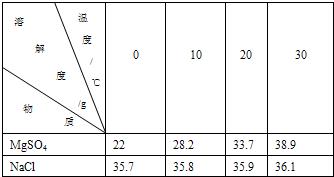
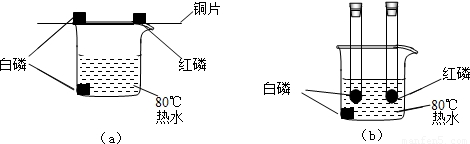
题目内容
(2008?淮安)请仔细观察下面四幅图象,其中能正确表示等质量的镁和铁分别与过量且相同溶质质量分数的稀硫酸反应的量的关系的是( )
【答案】分析:写出镁和铁分别与过量稀硫酸反应的方程式,可知相同质量的这两种金属完全反应时,镁产生的氢气多,且消耗完时所用的时间短.相同质量的镁与铁完全反应时,镁消耗的盐酸多.
解答:解:等质量的镁和铁可设为1g
Fe+2HCl=FeCl2+H2↑ Mg+2HCl=MgCl2+H2↑
56 73 2 24 73 2
1g Y1X11g Y2X2
X1= ,X2=
,X2=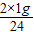
Y1=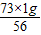 ,Y2=
,Y2=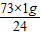
由此可得相同质量的镁和铁产生的氢气质量镁大于铁;
消耗的盐酸的质量镁大于铁;
故选C
点评:在金属活动顺序表中镁的位置排在铁的前边,所以镁的反应速度比铁快,用的时间短.
解答:解:等质量的镁和铁可设为1g
Fe+2HCl=FeCl2+H2↑ Mg+2HCl=MgCl2+H2↑
56 73 2 24 73 2
1g Y1X11g Y2X2
X1=
 ,X2=
,X2=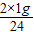
Y1=
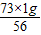 ,Y2=
,Y2=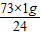
由此可得相同质量的镁和铁产生的氢气质量镁大于铁;
消耗的盐酸的质量镁大于铁;
故选C
点评:在金属活动顺序表中镁的位置排在铁的前边,所以镁的反应速度比铁快,用的时间短.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
(2008?淮安)同学们已经学习了一些金属的有关知识,对金属的活动性顺序也有了一定的认识.请运用所学知识参与以下探究并回答相关问题:
(1)将4枚洁净无锈的铁钉分别放入下面(a)、(b)、(c)、(d)4支试管中.再分别在(a)中加入少量的蒸馏水,(b)中加入少量的氯化钠溶液,(c)中注满迅速冷却的沸水,塞紧橡皮塞,(d)中加入少量干燥剂,再放入一团棉花球,把铁钉放在干棉花球上,塞紧橡皮塞(如图所示).
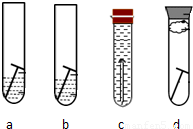
上述实验中,______试管中的铁钉最易生锈.设计如题图(d)实验的目的是______.
(2)某兴趣小组利用仅提供的铁、铜、硝酸银溶液三种药品探究铁、铜、银的金属活动性顺序.甲同学设计了如图(e)、(f)所示的两个实验: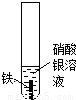
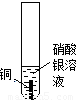
通过(e)实验得出的结论是______,(f)实验中观察到溶液的颜色由无色变为______色.乙同学认为甲同学设计的实验并不能达到实验目的,经过思考,他仍用这三种药品设计实验,并得出正确的结论.请你帮他完成实验报告:
列举上述探究结果在生产生活中的一条具体应用______.
(1)将4枚洁净无锈的铁钉分别放入下面(a)、(b)、(c)、(d)4支试管中.再分别在(a)中加入少量的蒸馏水,(b)中加入少量的氯化钠溶液,(c)中注满迅速冷却的沸水,塞紧橡皮塞,(d)中加入少量干燥剂,再放入一团棉花球,把铁钉放在干棉花球上,塞紧橡皮塞(如图所示).

上述实验中,______试管中的铁钉最易生锈.设计如题图(d)实验的目的是______.
(2)某兴趣小组利用仅提供的铁、铜、硝酸银溶液三种药品探究铁、铜、银的金属活动性顺序.甲同学设计了如图(e)、(f)所示的两个实验:


通过(e)实验得出的结论是______,(f)实验中观察到溶液的颜色由无色变为______色.乙同学认为甲同学设计的实验并不能达到实验目的,经过思考,他仍用这三种药品设计实验,并得出正确的结论.请你帮他完成实验报告:
| 操作 | 现象 | 结论 |
| 将铁片和铜片同时插入同一份硝酸银溶液中.然后将有明显现象的金属取出,继续观察另一金属片对应现象 | 一会,铁片表面明显变白,而铜片表面无明显现象.当铁片取出后,铜表面也慢慢变白. | 三种金属的活动性有强到弱的顺序:铁铜银 |