题目内容
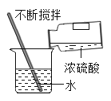
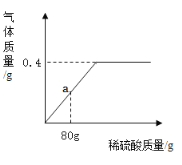
【题目】某兴趣小组用20g铁铜合金与质量分数为10%的稀硫酸充分反应,实验操作如下图所示,实验过程中产生气体的质量与稀硫酸的质量关系如下图所示:
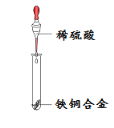
(1)左图中观察到的现象出产生气泡外,还有_______(填序号)。
A固体减少 B溶液由无色变为浅绿色 C溶液由无色变为蓝色
(2)右图中a点对应的稀硫酸中溶质的质量为____________g。
(3)计算铁铜合金中铁的质量分数(写出完整计算过程)。_________
【答案】AB 8 56%
【解析】
(1)根据金属活动性顺序表,稀硫酸和铁反应生成硫酸亚铁和氢气,稀硫酸不和铜反应。故反应现象为固体减少、溶液由无色变为浅绿色。故选AB。
(2)a点对应的稀硫酸中溶质的质量为10%×80g=8g。
(3)解:设参与反应的铁的质量为xg,
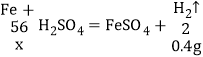
![]()
解得:x=11.2g
则铁铜合金中铁的质量分数![]() ×100%=56%。
×100%=56%。

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目