题目内容
【题目】小明模拟旅游时汽车穿越山洞的情境,设计了一个游戏。游戏规则:当汽车上的物质与山洞中的物质能发生反应时,汽车才能载着原物质进入下一个山洞。山洞中可供选择的物质有:稀硫酸、碳酸钠、氧化铁、氢氧化钠、镁、二氧化碳。
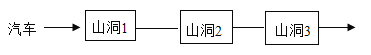
(1)若汽车上的物质是盐酸。
①山洞1中的物质是单质,该物质的化学式是_____。
②山洞2中的物质与盐酸反应后,溶液呈黄色,反应的化学方程式为_____。
③山洞3中的物质可以与盐酸发生复分解反应,产生无色气体。该反应的化学方程式为_____
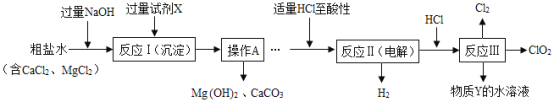
(2)若汽车上的物质是氢氧化钙。山洞1中的物质为氧化物,则山洞2、3中的物质是____,山洞1中反应的化学方程式为_____。
【答案】Mg Fe2O3 + 6HCl=2FeCl3 + 3H2O Na2CO3+ 2HCl=2NaCl + CO2↑+ H2O Na2CO3、H2SO4 CO2+ Ca(OH)2=CaCO3↓ + H2O
【解析】
由图可知,汽车穿越了三个山洞,所以汽车上的物质能与三个山洞中的物质反应。
(1)若汽车上的物质是盐酸,山洞中可供选择的物质有:稀硫酸、碳酸钠、氧化铁、氢氧化钠、镁、二氧化碳。
①山洞1中的物质是单质,根据游戏规则,符合条件的单质应该是镁,镁能与盐酸反应生成氯化镁和氢气,镁的化学式是Mg。故填:Mg。
②山洞2中的物质与盐酸反应后,溶液呈黄色,根据溶液颜色黄色判断山洞2中与盐酸反应的物质为氧化铁,生成的氯化铁溶液是黄色,反应的化学方程式为Fe2O3 + 6HCl=2FeCl3 + 3H2O。故填:Fe2O3 + 6HCl=2FeCl3 + 3H2O。
③山洞3中的物质可以与盐酸发生复分解反应,产生无色气体,碳酸钠与盐酸反应会生成二氧化碳气体,所以碳酸钠符合条件,它与盐酸反应的化学方程式为:Na2CO3+ 2HCl=2NaCl + CO2↑+ H2O。故填:Na2CO3+ 2HCl=2NaCl + CO2↑+ H2O。
(2)若汽车上的物质是氢氧化钙。山洞1中的物质为氧化物,能与氢氧化钙反应的氧化物就是二氧化碳,二者反应生成碳酸钙和水,反应的方程式为CO2+ Ca(OH)2=CaCO3↓ + H2O;山洞中可供选择的物质有:稀硫酸、碳酸钠、氧化铁、氢氧化钠、镁、二氧化碳,除了二氧化碳外,能与氢氧化钙反应的物质有碳酸钠和稀硫酸,则山洞2中、3中的物质是碳酸钠和稀硫酸。故填:Na2CO3、H2SO4;CO2+ Ca(OH)2=CaCO3↓ + H2O。

【题目】如图表示某个化学反应过程中各物质质量与时间的关系,下列描述正确的是
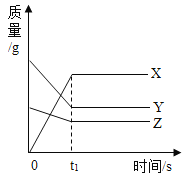
A.该反应是分解反应
B.X是反应物,Y和Z是生成物
C.t1时刻,反应物完全消耗完
D.t1时刻,X的质量等于Y和Z减少的质量之和
【题目】下列4个图像中,能正确反映对应变化关系的是
|
|
|
|
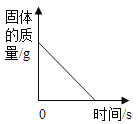
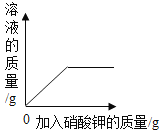
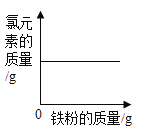
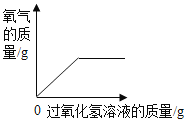
A.加热一定质量的高锰酸钾固体 | B.某温度下,向硝酸钾溶液中加入硝酸钾固体 | C.向一定质量的稀盐酸中加入铁粉 | D.向一定质量的二氧化锰中加入过氧化氢溶液 |
A.AB.BC.CD.D
【题目】同学们通过学习知道铜与盐酸、稀硫酸不能发生反应,但却发现化学老师用铜与浓硝酸制备出了NO2气体去做物理实验。同学们对此很感兴趣,在实验室对铜与硝酸的反应进行了探究。
实验I | 实验II | ||
实验装置 | 实验现象 | 实验装置 | 实验现象 |
| 铜片逐渐消失, 有无色气泡产生,试管中上部有红棕色气体出现;溶液由无色变为蓝色 |
| 铜片逐渐消失, 产生红棕色气体,溶液由无色变为绿色 |
(探究一)实验I中产生的无色气体是什么?
(查阅资料)
(1)硝酸(HNO3)与Cu反应生成硝酸铜和含氮元素的化合物;硝酸铜溶液呈蓝色
(2)含氮元素的某些气态物质的物理性质
NH3 | NO | NO2 | |
颜色 | 无色 | 无色 | 红棕色 |
气味 | 刺激性 | 刺激性 | |
溶解性 | 极易溶于水 | 难溶于水 | 可溶于水或硝酸 |
(3)NO2与水反应生成无色的硝酸和NO气体
(猜想与假设)无色气体可能是:①NH3 ②NO
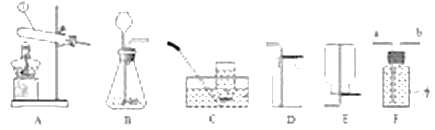
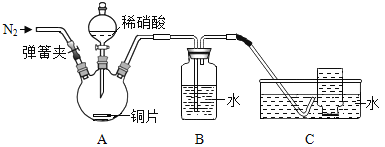
(进行实验)同学们利用下图装置对产生的无色气体进行检验。
实验操作 | 实验现象 |
1. 打开弹簧夹,通入N2,一段时间后,关闭弹簧夹 | B、C中导管口有无色气泡冒出 |
2. 将C中导管伸入集气瓶中,打开分液漏斗的活塞,滴入一定量稀硝酸,关闭活塞 | A中有无色气泡产生 B中导管口有无色气泡冒出 C中集气瓶内收集到无色气体 |
3. 从水槽中取出集气瓶,敞口置于空气中 | 无色气体变为红棕色 |
4. 取少量B中液体于试管中,滴加无色酚酞溶液 | 试管中溶液颜色无明显变化 |
(解释与结论)
(1)操作1中,通入N2的目的是_____。
(2)同学们认为猜想①不正确,理由是_____。
(3)无色气体具有的化学性质是_____。
(探究二)为什么实验II中的溶液呈绿色而不是蓝色?
(猜想与假设)①溶液中硝酸铜的质量分数较高②硝酸铜溶液中溶解了生成的气体
(设计实验)同学们设计了以下4个实验方案。
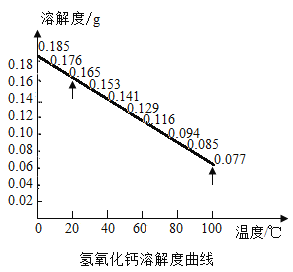
方案1 | 配制饱和硝酸铜溶液并稀释至不同的浓度,观察溶液颜色变化 |
方案2 | 加水稀释实验II所得的绿色溶液,观察溶液颜色变化 |
方案3 | 取实验II所得的绿色溶液,加热,观察溶液颜色变化 |
方案4 | 配制饱和硝酸铜溶液,…… |
(反思与评价)
(1)“方案1”和“方案3”中,能验证猜想②的是_____。
(2)“方案2”不能验证猜想①的原因是_____。
(3)“方案4”也可验证猜想②,该方案是:配制饱和硝酸铜溶液,_____。
(4)通过实验I、II与已有知识的对比,可得出的结论是_____(答一条即可)。