题目内容
小强发现家里有一包纯碱(包装说明如右下图),为了验证该纯碱的纯度,他把家里一小包纯碱样品带回学校进行实验:他准确称取5.5 g样品放入烧杯中,滴加盐酸至刚好完全反应(忽略CO2溶于水)时,共用去稀盐酸25 g,称得反应后溶液的质量为28.3 g(杂质溶于水且与盐酸不反应)
请计算:
(1)生成CO2的质量是 ;
(2)该纯碱样品中碳酸钠的质量分数为多少?
(计算结果精确到0.1%)
|
(1)2.2 g(2分)
(2)解:设5.5 g样品中含有碳酸钠的质量为x
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 44
x 2.2 g
106︰44=x︰2.2 g
解得x=5.3 g (2分)
则样品中碳酸钠的质量分数为![]() =96.4% (2分)
=96.4% (2分)

练习册系列答案
相关题目
 小强发现家里有一包纯碱(包装说明如右下图),为了验证该纯碱的纯度,他把家里一小包纯碱样品带回学校进行实验:他准确称取5.5g样品放入烧杯中,滴加盐酸至刚好完全反应(忽略CO2溶于水)时,共用去稀盐酸25g,称得反应后溶液的质量为28.3g(杂质溶于水且与盐酸不反应)
小强发现家里有一包纯碱(包装说明如右下图),为了验证该纯碱的纯度,他把家里一小包纯碱样品带回学校进行实验:他准确称取5.5g样品放入烧杯中,滴加盐酸至刚好完全反应(忽略CO2溶于水)时,共用去稀盐酸25g,称得反应后溶液的质量为28.3g(杂质溶于水且与盐酸不反应) 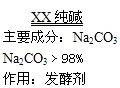 请计算:
请计算:
