题目内容
【题目】写出下列反应的化学方程式。
(1)镁条在氧气中燃烧________________;(2)铁在氧气中燃烧_______________;(3)高锰酸钾受热分解_______________;(4)氯酸钾与二氧化锰共热_______________;(5)氯化铵和氢氧化钠在加热时反应,生成氯化钠、有刺激性气味的气体氨气和水,写出该反应的化学方程式__________________。
【答案】2Mg+O2![]() 2MgO 3Fe+2O2
2MgO 3Fe+2O2![]() Fe3O4 2KMnO4
Fe3O4 2KMnO4![]() K2MnO4+MnO2+O2↑ 2KClO3
K2MnO4+MnO2+O2↑ 2KClO3![]() 2KCl+3O2↑ NH4Cl+NaOH
2KCl+3O2↑ NH4Cl+NaOH![]() NaCl+H2O+NH3↑
NaCl+H2O+NH3↑
【解析】
(1)镁条在氧气中燃烧生成氧化镁,反应的化学方程式为:2Mg+O2![]() 2MgO;
2MgO;
(2)铁在氧气中燃烧生成四氧化三铁,反应的化学方程式为:3Fe+2O2![]() Fe3O4;
Fe3O4;
(3)高锰酸钾受热后生成锰酸钾、二氧化锰和氧气,反应的化学方程式是2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(4)氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,反应的化学方程式为:2KClO3![]() 2KCl+3O2↑;
2KCl+3O2↑;
(5)氯化铵和氢氧化钠在加热时反应,生成氯化钠、有刺激性气味的气体氨气和水,写出该反应的化学方程式为NH4Cl+NaOH![]() NaCl+H2O+NH3↑;
NaCl+H2O+NH3↑;
故答案为:(1)2Mg+O2![]() 2MgO;(2)3Fe+2O2
2MgO;(2)3Fe+2O2![]() Fe3O4;(3)2KMnO4
Fe3O4;(3)2KMnO4![]() K2MnO4+MnO2+O2↑;(4)2KClO3
K2MnO4+MnO2+O2↑;(4)2KClO3![]() 2KCl+3O2↑;(5)NH4Cl+NaOH
2KCl+3O2↑;(5)NH4Cl+NaOH![]() NaCl+H2O+NH3↑.
NaCl+H2O+NH3↑.

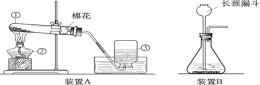
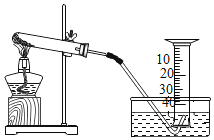
【题目】某兴趣小组对KClO3分解反应的催化剂进行研究,在相同的加热条件下,用如图装置完成表中实验:
编号 | KClO3质量/g | 催化剂 | 催化剂质量/g | 收集50 mL O2所需时间/s |
实验1 | 5 | - | - | 171 |
实验2 | 5 | MnO2 | 0.5 | 49 |
实验3 | 5 | Fe2O3 | 0.5 | 58 |
实验4 | 5 | KCl | 0.5 | 154 |
(1)设置实验1的目的是________。
(2)表中所列3种催化剂的催化效果最佳的是_____。
(3)写出KClO3分解的符号表达式:______________________。
(4)由实验1和实验4可知,KCl__(填“有”或“无”)催化作用。维持加热条件不变,用实验1再继续收集50 mL O2,所需时间明显少于171 s,解释原因:_______。
(5)要比较KClO3分解反应中不同催化剂的催化效果,除了测量收集50 mL O2所需时间外,还可以测量相同时间内____________。