题目内容
(2009?营口模拟)我市濒临渤海,有丰富的海水资源;东部山区有丰富的石灰石,以海水和生石灰为原料可以制取生产镁的原料MgCl2.
模拟化工厂的生产流程:
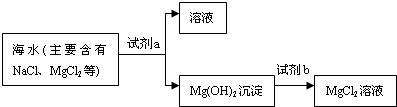
①试剂a是一种溶液,其溶质是
②加入试剂a后,要将Mg(OH)2沉淀分离出来,应该应用的方法是
学校实验室中完成该实验,需要的玻璃仪器除烧杯、玻璃棒外还有
③流程中加入的 试剂b是
模拟化工厂的生产流程:

①试剂a是一种溶液,其溶质是
Ca(OH)2
Ca(OH)2
(填化学式).②加入试剂a后,要将Mg(OH)2沉淀分离出来,应该应用的方法是
过滤
过滤
,如果在学校实验室中完成该实验,需要的玻璃仪器除烧杯、玻璃棒外还有
漏斗
漏斗
.③流程中加入的 试剂b是
盐酸
盐酸
.分析:此题的实质是将MgCl2从NaCl和MgCl2的混合物溶液中分离出来,其基本的方法是将MgCl2转化为Mg(OH)2沉淀,过滤分离出Mg(OH)2后再复原.
(1)为了使MgCl2转化为Mg(OH)2沉淀,所加的试剂选择为Ca(OH)2,Ca(OH)2 来源广泛,成本低,可以和MgCl2反应,生成Mg(OH)2;(2)过滤是一种常见的分离混合物的方法,能将固体和液体分开,过滤过程中需要用到烧杯、玻璃棒、漏斗、铁架台这些仪器;(3)氢氧化镁属于沉淀,只能用酸来溶解,不能引入新的杂质,所以加入盐酸即可.
(1)为了使MgCl2转化为Mg(OH)2沉淀,所加的试剂选择为Ca(OH)2,Ca(OH)2 来源广泛,成本低,可以和MgCl2反应,生成Mg(OH)2;(2)过滤是一种常见的分离混合物的方法,能将固体和液体分开,过滤过程中需要用到烧杯、玻璃棒、漏斗、铁架台这些仪器;(3)氢氧化镁属于沉淀,只能用酸来溶解,不能引入新的杂质,所以加入盐酸即可.
解答:解:(1)试剂a应该选择Ca(OH)2溶液,它能把MgCl2反应转化成为Mg(OH)2沉淀,而且本身来源广泛,价格便宜,可以节约成本.
(2)加入试剂后,要将Mg(OH)2沉淀分离出来,应该应用的方法是过滤,达到把混合液中固体和液体分开的目的.过滤用到的玻璃仪器除了烧杯、玻璃棒,还需要漏斗;
(3)氢氧化镁属于沉淀,只能用酸来溶解,不能引入新的杂质,所以加入盐酸即可,盐酸与氢氧化镁反应生成氯化镁和水..
故答案为:①Ca(OH)2;②过滤;漏斗;③盐酸.
(2)加入试剂后,要将Mg(OH)2沉淀分离出来,应该应用的方法是过滤,达到把混合液中固体和液体分开的目的.过滤用到的玻璃仪器除了烧杯、玻璃棒,还需要漏斗;
(3)氢氧化镁属于沉淀,只能用酸来溶解,不能引入新的杂质,所以加入盐酸即可,盐酸与氢氧化镁反应生成氯化镁和水..
故答案为:①Ca(OH)2;②过滤;漏斗;③盐酸.
点评:此题以实验流程图的形式,呈现探究海水中氯化镁的提取过程,以实验流程图呈现实验过程,是近几年中考探究命题特点之一.读懂实验流程图,明确实验步骤和原理,是正确解答此类问题的前提.

练习册系列答案
相关题目
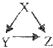 (2009?营口模拟)下列各组物质能按照关系图(→表示反应一步完成)相互转化的是( )
(2009?营口模拟)下列各组物质能按照关系图(→表示反应一步完成)相互转化的是( )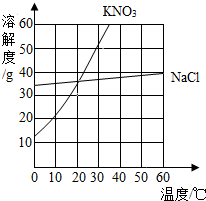 (2009?营口模拟)某同学根据如图所示的溶解度曲线得以下信息,其中正确的是( )
(2009?营口模拟)某同学根据如图所示的溶解度曲线得以下信息,其中正确的是( )